
| X | ||
| Y | ||
| Z |
| A. | X是活泼的非金属元素,其最高价氧化物的水化物是一种强酸 | |
| B. | Y是最活泼的非金属元素,不存在最高价氧化物的水化物 | |
| C. | Z是较活泼的非金属元素,其最高价氧化物的水化物是一种强酸 | |
| D. | X、Y、Z的单质中Z的熔点最高 |
分析 由三种短周期元素在周期表中的位置关系可知,X为He、Y为氟元素、Z为硫元素,
A.He为稀有气体,没有最高价氧化物;
B.F元素没有最高正价;
C.硫酸为强酸;
D.硫常温下为固体.
解答 解:由三种短周期元素在周期表中的位置关系可知,X为He、Y为氟元素、Z为硫元素,
A.He为稀有气体,活泼性很弱,没有最高价氧化物,故A错误;
B.F是最活泼的非金属元素,F元素没有最高正价,即不存在最高价氧化物的水化物,故B正确;
C.Z为S元素,其最高价氧化物的水化物硫酸为强酸,故C正确;
D.He、F的单质常温下为气体,S的单质为固体,所以X、Y、Z的单质中Z的熔点最高,故D正确.
故选A.
点评 本题考查结构性质位置关系、元素周期律等,难度不大,注意整体把握元素周期表的结构.


科目:高中化学 来源: 题型:多选题

| A. | 甲装置:用所示装置分离出溴苯 | |
| B. | 乙装置:加热浓硫酸和乙醇混合液,制取乙烯 | |
| C. | 丙装置:加热苯和硝基苯的混合物,分离出苯 | |
| D. | 丁装置:验证溴乙烷发生消去反应生成烯烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
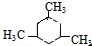 .
.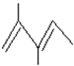 .
.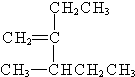 3-甲基-2-乙基-1-戊烯;
3-甲基-2-乙基-1-戊烯; 2,2,6-三甲基-4-乙基辛烷.
2,2,6-三甲基-4-乙基辛烷.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
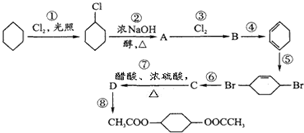 从环己烷可制备1,4-环己二醇二醋酸酯,下列过程是有关的8步反应(其中所有无机产物都已略去):
从环己烷可制备1,4-环己二醇二醋酸酯,下列过程是有关的8步反应(其中所有无机产物都已略去): ,C
,C ,D
,D .
.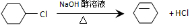 ;
; ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X为0.25 mol•L-1 | |
| B. | Y为0.1 mol•L-1 | |
| C. | Z为0.2 mol•L-1 | |
| D. | Z为0.25 mol•L-1时,Y为0.45 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠的还原性很强,可以用来冶炼金属钛、锆、铌等 | |
| B. | 钠的化学性质非常活泼,钠元素只能以化合态存在于自然界 | |
| C. | 钠极易和水反应而被还原 | |
| D. | 钠、氧化钠、氢氧化钠的焰色反应均显黄色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com