
【题目】一定条件下,将amolA与15molB的混合气体通入一固定体积为5L的密闭容器中,发生如下反应:A(g)+3B(g)![]() 2C(g)
2C(g)
(1)若反应进行到10min时达到平衡,n1(A)=13mol,n1(C)=6mol,;计算a的值___;这段时间内的C平均反应速率为___。
(2)反应达平衡时,B的转化率为分别为___;A的体积分数为___。
(3)下列操作能使该反应的反应速率增大的是___。
A.向密闭容器中通入氦气增大压强
B.增大A的浓度
C.适当升高温度
D.将容器的体积扩大至10L
(4)反应过程中容器内气体的密度是___(填“增大”、“减小”或“不变”,下同),平均相对分子质量是___。
【答案】16mol 0.12molL-1min-1 60% 52% BC 不变 增大
【解析】
从已知条件列出反应的三段式: 。
。
(1)根据反应方程式,生成6molC,则消耗![]() ,反应初始
,反应初始![]() ;这段时间内的C平均反应速率为
;这段时间内的C平均反应速率为![]() ;故答案为:16mol;0.12molL-1min-1;
;故答案为:16mol;0.12molL-1min-1;
(2)反应达平衡时的三段式:

B的转化率为:![]() ;A的体积分数为:
;A的体积分数为:![]() ;故答案为:60%;52%;
;故答案为:60%;52%;
(3) A.该反应为恒容密闭容器,通入氦气,但反应物的浓度不变,化学反应速率不变,A错误;
B.A是气体,增大A的浓度,即增大反应物的浓度,能加快化学反应速率,B正确;
C.适当升高温度,化学反应速率加快,C正确;
D.将容器的体积扩大至10L,反应物的浓度减小,化学反应速率减慢,D错误;
答案选BC。
(4)该反应在恒容密闭容器内进行,体积不变,体系内的物质全是气体,故总质量不变,则反应过程中容器内气体的密度是不变的;该反应气体物质的量减小,而质量不变,故平均相对分子质量是增大的;答案为:不变;增大。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某有机物A的分子式为C4H8O2,已知A~E有下列转化关系如下,试回答下列问题:

(1)C中的官能团名称是_______;
(2)E的结构简式是_______。
(3)在图中①~④的反应中,属于氧化反应的有________。
(4)写出反应②的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对化学用语的理解中正确的是( )
A.原子结构示意图:![]() 可以表示35Cl,也可以表示37Cl
可以表示35Cl,也可以表示37Cl
B.电子式:![]() 可以表示羟基,也可以表示氢氧根离子
可以表示羟基,也可以表示氢氧根离子
C.比例模型![]() :可以表示甲烷分子,也可以表示四氯化碳分子
:可以表示甲烷分子,也可以表示四氯化碳分子
D.结构简式(CH3)2CHOH:可以表示1-丙醇,也可以表示2-丙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ⑥ | ⑦ | ⑧ | |||||
3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
4 | ② | ④ |
(1) 在③~⑦元素中,原子半径最大的是__________(填元素符号);
(2) ⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有________________________;
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:_____________。
(4) ③、⑤、⑦、⑧形成的离子,其半径由小到大的顺序是________(填离子符号)
(5) ①~⑨中元素最高价氧化物对应的水化物中酸性最强的是_____________(填物质化学式),呈两性的氢氧化物是_________(填物质化学式);该化合物与NaOH溶液反应的离子方程式为___________。
(6) 用电子式表示元素③与⑨形成化合物的过程_____________________________。
(7)写出工业冶炼⑤的化学方程式:_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应S2O82-(aq)+2I-(aq)![]() 2SO42-(aq)+I2(aq),若往该溶液中加人含Fe3+的某溶液,反应机理:①2Fe3++(aq)+2I-(aq)
2SO42-(aq)+I2(aq),若往该溶液中加人含Fe3+的某溶液,反应机理:①2Fe3++(aq)+2I-(aq)![]() I2(aq)+2Fe2+(aq)②2Fe2+(aq)+S2O82-(aq)
I2(aq)+2Fe2+(aq)②2Fe2+(aq)+S2O82-(aq) ![]() 2Fe3+(aq)+2SO42-(aq),下列有关该反应的说法不正确的是
2Fe3+(aq)+2SO42-(aq),下列有关该反应的说法不正确的是
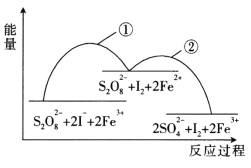
A.增大S2O82-浓度或I-浓度,反应①、反应②的反应速率均加快
B.Fe3+是该反应的催化剂
C.因为正反应的活化能比逆反应的活化能小,所以该反应是放热反应
D.往该溶液中滴加淀粉溶液,溶液变蓝,适当升温,蓝色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某研究性学习小组设计制取氯气并以氯气为反应物进行特定反应的装置。
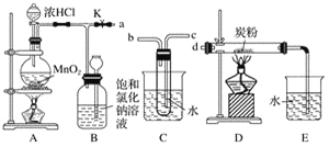
(1)①盛装浓盐酸的仪器名称为___,盛装二氧化锰的仪器名称为___。
②请写出装置A中发生反应的化学方程式___。
③标准状况下,上述反应每生成2.24L氯气,转移电子的物质的量为___mol。
(2)要将C装置接入B和D之间,正确的接法是:a→___→___→d。
(3)实验开始先点燃A处的酒精灯,打开活塞K,让Cl2充满整个装置,再点燃D处的酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为___。
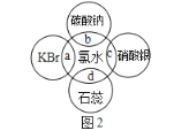
(4)氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图2所示四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。
①能证明氯水具有漂白性的是___(填“a”“b”“c”或“d”)。
②c过程中的现象是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成药物中间体L的路线如图(部分反应条件或试剂略去):
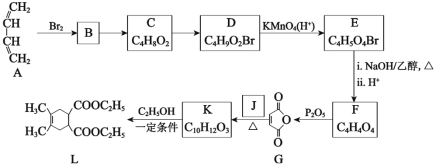
已知:I.最简单的Diels-Alder反应是![]()
II.![]()
III.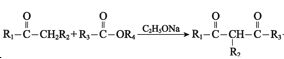 +R4OH
+R4OH
请回答下列问题:
(1)下列说法中正确的是____。
A.B→C的反应条件可以是“NaOH/H2O,△”
B.C→D的目的是实现基团保护,防止被KMnO4(H+)氧化
C.欲检验化合物E中的溴元素,可向其中滴加HNO3酸化的AgNO3溶液观察是否有淡黄色沉淀生成
D.合成药物中间体L的分子式是C14H20O4
(2)写出化合物J的结构简式____。
(3)写出K→L的化学方程式____。
(4)设计由L制备M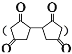 的合成路线(用流程图表示,试剂任选)____。
的合成路线(用流程图表示,试剂任选)____。
(5)写出化合物K同时符合下列条件的同分异构体的结构简式____。
①1H-NMR谱检测表明:分子中共有5种化学环境不同的氢原子;
②能发生水解反应;
③遇FeCl3溶液发生显色反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以甲苯为原料,设计以下路径合成药物中间体M和R。回答下列问题:
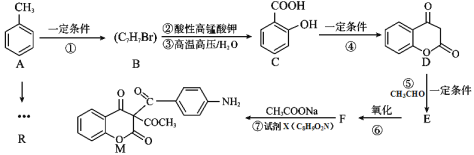
已知:①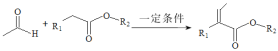
②![]()
③![]()
(1)C中的官能团的名称为______,F的结构简式为______,A→B的反应类型为_______。
(2)D→E的反应方程式为______________________________________。
(3)M物质中核磁共振氢谱中有________组吸收峰。
(4)至少写出2个同时符合下列条件试剂X的同分异构体的结构简式_________________
①只有一个苯环且苯环上的一氯取代物只有2种 ②遇FeCl3溶液显紫色 ③分子中含![]()
(5)设计由甲苯制备R(![]() )的合成路线(其它试剂任选)。______________________________
)的合成路线(其它试剂任选)。______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置不能达到实验目的的是
A.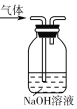 用装置除去乙烯中的少量酸性气体
用装置除去乙烯中的少量酸性气体
B.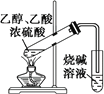 用装置完成实验室制取乙酸乙酯
用装置完成实验室制取乙酸乙酯
C. 用装置证明温度对化学平衡的影响
用装置证明温度对化学平衡的影响
D.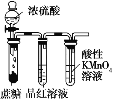 用装置验证浓硫酸具有脱水性、强氧化性,SO2具有漂白性、还原性
用装置验证浓硫酸具有脱水性、强氧化性,SO2具有漂白性、还原性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com