
| A. | 二氧化硫和二氧化碳都能使澄清的石灰水变浑浊 | |
| B. | 二氧化硫通入BaCl2溶液中生成BaSO3白色沉淀 | |
| C. | 二氧化硫通入滴有酚酞的NaOH溶液中,红色褪去,说明二氧化硫具有漂白性 | |
| D. | 硫在过量的氧气中燃烧生成三氧化硫 |
分析 A.二氧化硫和二氧化碳与氢氧化钙反应生成亚硫酸钙和碳酸钙;
B.盐酸的酸性强于亚硫酸;
C.二氧化硫为酸性氧化物;
D.硫在氧气中燃烧生成二氧化硫.
解答 解:A.二氧化硫和二氧化碳与氢氧化钙反应生成亚硫酸钙和碳酸钙,二者都不溶于水,故A正确;
B.盐酸的酸性强于亚硫酸,二氧化硫通入BaCl2溶液不会发生反应,故B错误;
C.二氧化硫为酸性氧化物,能够与氢氧化钠反应,二氧化硫通入滴有酚酞的NaOH溶液中,红色褪去,体现二氧化硫酸性氧化物的性质,故C错误;
D.硫在氧气中燃烧生成二氧化硫,故D错误;
故选:A.
点评 本题考查了物质的性质,熟悉二氧化硫的性质是解题关键,注意二氧化硫的还原性、酸性氧化物的性质、漂白性,题目难度不大.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:解答题
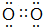 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
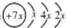 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醛的分子式:C2H4O | B. | 苯的结构简式: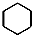 | ||
| C. | 乙炔的结构简式:CH≡CH | D. | 乙醇的结构简式:C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+ | B. | H2O2 | C. | Cl2 | D. | ClO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
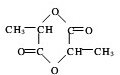 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6CO2+6H2O$\stackrel{光合作用}{→}$C6H12O6+6O2 | B. | CO2+CH4$→_{△}^{催化剂}$CH3COOH | ||
| C. | CO2+3H2$→_{△}^{催化剂}$CH3OH+H2O | D. | 2CO2+6H2$→_{△}^{催化剂}$CH2=CH2+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 具有下列电子排布式的原子中,①1s22s22p63s2;②1s22s22p63s23p1;第一电离能:①>② | |
| B. | 某元素气态基态原子的逐级电离能(kJ•mol-1)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X3+ | |
| C. | 具有下列价电子排布式的原子中,①3s23p2②2s22p3:原子半径①>② | |
| D. | Na、P、Cl三种元素的电负性依次增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com