
A、B、C、D、E五种元素均为短周期元素,原子序数逐渐增大。A形成的单质密度最小(相同条件下)。B可形成多种同素异形体,其中一种的硬度自然界中最大。D元素原子的最外层电子数是次外层电子数的3倍。E元素的最高价氧化物的水化物的酸性强于硫酸。
(1)元素C位于元素周期表的 周期 族,原子结构示意图为 。
(2)B、C、D三种元素的最简单氢化物的稳定性从大到小的顺序是 (填化学式),BE4分子的空间构型是 。
(3)元素A与B形成原子个数比为1:1的相对分子质量最小的化合物的结构式为 。
(4)A、B、C、D几种元素之间可以形成多种10电子微粒,写出上述10电子微粒之间反应的其中一个化学方程式或离子方程式:
(5)写出E的单质制取漂白粉反应的化学方程式并标出电子转移的方向和数目:
(共16分)
(1)二 VA (2分)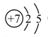 (2分),
(2分),
(2)H2O>NH3>CH4(2分) 正四面体(2分)
(3)  (2分)
(2分)
(4)NH3+H2O=NH3·H2O或OH-十NH4+=NH3·H2O(2分)
(5)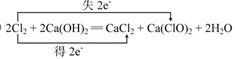 (化学方程式2分,电子转移2分,共4分)
(化学方程式2分,电子转移2分,共4分)
解析试题分析:根据题意可以推断A、B、C、D、E分别为H、C、N、O、Cl。10个电子的离子可以以氖为中心,氖前面的阴离子和氖后面的阳离子以及阴离子对应的氢化物、氢化物的阴阳离子等。H、C、N、O想到CH4、NH3(NH2-、NH4+)、H2O(H3O+、OH-)、HF等。Cl2与漂白粉的反应为歧化反应,在表电子转移是最好使用单线桥法(参考答案以及2012安徽高考卷均使用双线桥法,不知何意)
考点:考查物质结构,涉及元素周期表结构、元素周期律、分子结构、氧化还原反应等相关知识。


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:填空题
A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。
请回答下列问题:
(1)元素D在周期表中的位置_______________________。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)___________.
(3)由A、B、C三种元素以原子个数比4 :2 :3形成化合物X,X中所含化学键类型有________________.
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:____________;若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:________________。
(5)FC2气体有毒,排放到大气中易形成酸雨,写出FC2与氧气和水蒸气反应的化学方________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
元素周期表是人们研究物质性质的重要工具,下表是元素周期表的一部分,请用化学用语回答下列问题: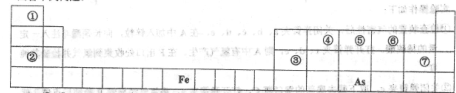
(1)①—⑦号元素原子半径最大的是____,最高价氧化物对应的水化物物酸性最强的是________________.
(2)写出由①-⑦号元素中的几种组成显碱性的盐的化学式____________________。(写出2种即可),并用离子方程式表示其中一种显碱性的原因____________________.
(3)写出③号元素的最高价氧化物与①-⑦号元素中金属性最强的元素的最高价氧化物的水化物反应的离子方程式_____________________。
(4) As在元素周期表中的位置是________________。
⑸As的原子结构示意图为________,其氢化物的电子式为___________.
(6)Y是由②⑥⑦三种元素组成,它的水溶液是一种生活中常见的消毒剂。As可以与Y的水溶液反应,生成其最高价含氧酸(H3AsO4 ),写出该反应的离子方程式_____________________,
当消耗1mol还原剂时转移电子的物质的量为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知A、B、C、D、E五种短周期元素,A的最外层电子数是其电子层数的3 倍,A、B同主族,C在短周期主族元素中原子半径最大,E2是黄绿色气体,D为金属元素,其单质可以用于工业冶炼Fe。
(1)D在周期表中的位置是______ ;
A、B、C离子半径由大到小的顺序为______ 。(用离子符号回答)
(2)工业上用E的单质制备漂白粉的化学方程式为
_____ _____ ;
将少量C2A2加入水中可观察到的实验现象是 ;向所得溶液中加入酚酞可观察到溶液先变红后褪色,由此说明溶液中有______ (填化学式)两种物质生成。
(3)D与Fe2O3的反应还可以用于定向爆破,其化学反应方程式为
__ ___ ;
该反应为______(填“吸热”或“放热”)反应。
(4)常温下,将0.0025 mol的BA2E2溶于水配成0.1L溶液,所得溶液的pH= 1,则 BA2E2与水反应的化学方程式为_______ _____。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D、E为前四周期中原子序数依次增大的元素,相关的信息如下:
| 元素 | 相关信息 |
| A | A元素原子核外只有三个能级,且每个能级上含有相等的电子数 |
| B | 是空气中含量最丰富的元素 |
| C | 短周期中,单质C的金属性最强 |
| D | 基态原子第三能层上有7种运动状态不同的电子 |
| E | 一种核素的质量数为63,中子数为34 |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下表中所列的字母分别代表某一化学元素。完成下列填空:
| a | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | b | | |
| c | | | | | | | | | | | | d | | | e | f | |
| | | | | | | | | | | | | | g | | | | |
| | | | | | | | | | | | | | | | h | | |
| | i | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y、Z、W是元素周期表前四周期常见的四种元素,原子序数依次增大。X的单质既有σ键乂有π键,且X的第一电离能比其相邻元素都大,Y的电负性比X的小,其基态原子最外层的p电子是该层s电子的两倍,Z是前36号元素中原子半径最大的主族元素,W的一种核素的质量数是56,中子数是30。
(1) Y位于元素周期表第_______周期第_______族,W2+的核外电子排布式是______。
(2) X的氧化物XO2与H2O比较,熔点较高的是_______ (填化学式),Z的氢化物属于 晶体,Z2O2的化学键类型是_______(填编号)
| A.离子键 | B.极性共价键 | C.非极性共价键 | D.金属键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图为元素周期表的一部分,根据元素①~⑧在周期表中的位置,按要求回答下列问题。
| 族 周期 | IA | | 0 | |||||
| 1 | ① | IIA | IIIA | ⅣA | VA | ⅥA | VIIA | |
| 2 | | | | | | ② | ③ | |
| 3 | ④ | ⑤ | | | | ⑥ | ⑦ | ⑧ |
| | 序号 | 条件 | 现象 | 结论 | |
| 温度/℃ | 催化剂 | ||||
| 第一组 | 1 | 40 | FeCl3溶液 | 快速产生大量气泡 | 相同条件下,温度升高,化学反应速率加快 |
| 2 | 20 | A | 缓慢产生适量气泡 | ||
| 3 | 5 | FeCl3溶液 | 缓慢产生极少量气泡 | ||
| 第二组 | 4 | t | MnO2 | 快速产生大量气泡 | |
| 5 | 20 | 无 | 缓慢产生极少量气泡 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
前四周期原子序数依次增大的元素A,B,C,D中,A和B的价电子层中未成对电子均只有1个,平且A—和B+的电子相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。
回答下列问题:
(1)D2+的价层电子排布图为_______。
(2)四种元素中第一电离最小的是________,电负性最大的是________。(填元素符号)
(3)A、B和D三种元素责成的一个化合物的晶胞如图所示。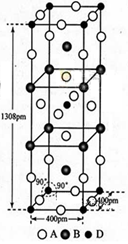
①该化合物的化学式为_________________;D的配位数为___________;
②列式计算该晶体的密度_______g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物B3CA6,其中化学键的类型有_________;该化合物中存在一个复杂离子,该离子的化学式为________,配位体是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com