
常温下,关于下列各溶液的叙述正确的是
| A.pH=7的醋酸钠和醋酸的混合溶液中:c(CH3COO-)>c(Na+) |
| B.0.1mol/L稀醋酸pH=a,0.01mol/L的稀醋酸pH=b,则a+1=b |
| C.0.1mol/L的醋酸钠溶液20mL与0.1mol/L的盐酸10mL混合后溶液显酸性:c(CH3COOH)-c(CH3COO-)=2[c(OH-)-c(H+)] |
| D.已知酸性HF>CH3COOH,pH相等的NaF溶液与CH3COOK溶液中:[c(Na+)-c(F-)] >[c(K+)-c(CH3COO-)] |
C
解析试题分析: A、醋酸钠与醋酸混合溶液中电荷守恒式为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),因pH=7,所以c(CH3COO-)=c(Na+),错误;B、醋酸溶液浓度越大,电离度越小,所以a+1>b,错误;C、0.1mol/L的醋酸钠溶液20mL与0.1mol/L的盐酸10mL混合后电荷守恒式为c(Na+)+c(H+)=c(CH3COO-)+c(OH-)+c(Cl-)、物料守恒式为c(CH3COO-)+c(CH3COOH)=c(Na+)。其中c(Na+)=2c(Cl-),将电荷守恒式乘以2与物料守恒式相加得c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-),正确;D、NaF和CH3COOK溶液中电荷守恒式分别为c(Na+)+c(H+)=c(F-)+c(OH-)、c(K+)+c(H+)=c(CH3COO-)+c(OH-),因两溶液pH相等,所以c(H+)和c(OH-)分别相等,所以[c(Na+)-c(F-)]=[c(K+)-c(CH3COO-)],错误。
考点: 离子浓度比较


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:单选题
下列判断正确的是
A.同温下,HF比HClO易电离,则NaF溶液的pH比NaClO溶液的pH大
B.常温下,0.4 mol?L-1 HA溶液和0.2 mol?L-1NaOH溶液等体积混合后的pH等于3,则混合溶液中粒子浓度大小关系:c(A-)>c(Na+)>c(HA)>c(H+)>c(OH—)
C.常温下,BaSO4在饱和Na2SO4溶液中的Ksp比在纯水中的Ksp小
D.用铂电极电解食盐水,一段时间后两极产生气体体积比为3:2(同条件下),为将电解液恢复原状,则只需向电解液中通入一定量的HCl气体
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,pH=8~9的Na2SO3溶液中存在:SO32ˉ+H2O HSO3ˉ+OHˉ,下列说法正确的是
HSO3ˉ+OHˉ,下列说法正确的是
| A.加入少量NaOH固体,Kw增大 |
| B.c(OHˉ)= c(HSO3ˉ)+2 c(H2SO3)+ c(H+) |
| C.c(SO32ˉ)> c(OHˉ) > c(HSO3ˉ) |
| D.加入稀盐酸,c(HSO3ˉ)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关电解质溶液中微粒的关系不正确的是
| A.25℃时,pH=4的氯化铵溶液中:c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| B.25℃时,pH=3的氯化铵溶液中: c(OH-)=1.0×10-11mol·L-1 |
| C.将pH=5的醋酸溶液稀释后,恢复至原温度,pH和Kw均增大 |
| D.向NH4HSO4溶液中加入等物质的量的NaOH形成的溶液中:c(Na+) = c(SO42-) >c(NH4+) >c(H+) > c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各溶液中,微粒的物质的量浓度关系正确的是
| A.0.1 mol·L-1 Na2CO3溶液:c(Na+)=2c(HCO3-)+2c(CO32¯)+2c(H2CO3) |
| B.0.1 mol·L-1 NH4Cl溶液:c(NH4+)=c(Cl-) |
| C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.常温下,将pH=2的盐酸和pH=12的氨水等体积混合后:c(NH4+)>c(Cl-)> c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,下列有关叙述正确的是
A.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合: |
B.Na2CO3溶液中, |
C.pH相等的CH3COONa、NaClO、NaHCO3三种溶液: |
D.NH4Cl溶液和NaOH溶液混合所得的中性溶液中: |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某温度下, pH值相同的盐酸和氯化铵溶液分别稀释,平衡pH值随溶液体积变化的曲线如下图所示。据图判断下列叙述中,正确的是( )
| A.Ⅱ为氯化铵稀释时pH值变化曲线,a点水的电离程度大于c点水的电离程度 |
| B.b点溶液中水的电离程度比c点溶液中水的电离程度大,且两点的KW相同 |
| C.a点时,等体积的两溶液与NaOH反应消耗的NaOH量相同 |
| D.加入足量NaOH,b点溶液消耗的NaOH比d点溶液消耗的多 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
能说明醋酸是弱电解质的事实是:
①用浓硫酸和醋酸钠固体共热可以制得醋酸,②醋酸钠水溶液呈碱性,
③可以用食醋清除水壶中的水垢,④pH=2的醋酸溶液稀释1000倍后的pH<5
| A.①③④ | B.①② | C.②④ | D.② |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
【化学与技术】
电镀厂镀铜废水中含有CN-和Cr2O72-离子,需要处理达标后才能排放。该厂拟定下列流程进行废水处理,回答下列问题: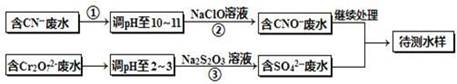
(1)上述处理废水流程中主要使用的方法是______。
(2)②中反应后无气体放出,该反应的离子方程式为 。
(3)步骤③中,每处理0.4mol Cr2O72-时转移电子2.4mol,该反应离子方程式为 。
(4)取少量待测水样于试管中,加入NaOH溶液,观察到有蓝色沉淀生成,再加Na2S溶液,蓝色沉淀转化成黑色沉淀,请使用化学用语和文字解释产生该现象的原因 。
(5)目前处理酸性Cr2O72-废水多采用铁氧磁体法。该法是向废水中加入FeSO4·7H2O将Cr2O72-还原成Cr3+,调节pH,Fe、Cr转化成相当于FeII[FeCr]O4(铁氧磁体,罗马数字表示元素价态)的沉淀。处理1mol Cr2O72-,需加入a mol FeSO4?7H2O,下列结论正确的是_______。
| A.x ="0.5" ,a =8 | B.x =0.5,a = 10 |
| C.x =" 1.5" ,a =8 | D.x =" 1.5" ,a = 10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com