
| A. | 1 L 0.1 mol•L-1 (NH4)2Fe(SO4)2•6H2O溶液中:c(NH4+)+c(Fe2+)+c(H+)=c(OH-)+c(SO42-) | |
| B. | 0.1 mol•L-1的NH4Cl与0.1 mol•L-1的NH3•H2O等体积混合:c(NH4+)+2c(H+)=c(NH3•H2O)+2c(OH-) | |
| C. | pH=9.4、浓度均为0.1 mol•L-1的HCN与NaCN的混合溶液中:c(Na+)>c(CN-)>c(HCN)>c(OH-) | |
| D. | 0.1 mol•L-1 CH3COONa 溶液与0.05 mol•L-1盐酸等体积混合后的酸性溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
分析 A、电荷守恒分析解答;
B、根据质子守恒分析解答;
C、pH=9.4说明溶液呈碱性,则HCN与NaCN的混合溶液水解程度大于电离程度;
D、0.1 mol•L-1 CH3COONa 溶液与0.05 mol•L-1盐酸等体积混合得到物质的量浓度相等的CH3COONa、CH3COOH和NaCl,由此分析解答.
解答 解:A、电荷守恒可知:c(NH4+)+2c(Fe2+)+c(H+)=c(OH-)+2c(SO42-),故A错误;
B、根据质子守恒,可知:c(NH4+)+2c(H+)=c(NH3•H2O)+2c(OH-),故B正确;
C、pH=9.4说明溶液呈碱性,则HCN与NaCN的混合溶液水解程度大于电离程度,所以离子浓度大小为:c(Na+)>c(HCN)>c(CN-)>c(OH-),故C错误;
D、0.1 mol•L-1 CH3COONa 溶液与0.05 mol•L-1盐酸等体积混合得到物质的量浓度相等的CH3COONa、CH3COOH和NaCl,溶液呈酸性,则电离大于水解,所以c(CH3COO-)>0.025 mol•L-1,c(Cl-)=0.025 mol•L-1,c(CH3COOH)<0.025 mol•L-1,则:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+),故D正确;
故选BD.
点评 本题考查盐类水解及弱电解质电离,明确弱电解质电离特点以及溶液中电荷守恒和物料守恒是解本题关键,题目难度中等,侧重于考查学生的分析能力.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 LNH3中含有的氢原子数为3NA | |
| B. | 标准状况下,足量Na2O2和11.2LCO2反应,转移电子数目为NA | |
| C. | 常温常压下,16g CH4中所含中子数为10NA | |
| D. | 常温常压下,2.8g乙烯中含有碳氢键的数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲硫醇(CH3SH)比甲醇(CH3OH)的熔点低的原因是甲醇分子间易形成氢键 | |
| B. | N-O键的极性比C-O键的极性小 | |
| C. | 氨易液化与氨分子间存在氢键有关 | |
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 青铜、不锈钢和硬铝都是合金 | |
| B. | 铝可用于制造燃烧弹和信号弹 | |
| C. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用,因此铝罐可久盛食醋 | |
| D. | 铜锈的主要成分是Cu2(OH)2CO3,可以用稀盐酸除铜锈 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
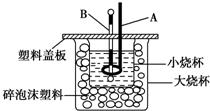 已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol.回答有关中和反应的问题.
已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol.回答有关中和反应的问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法正确的是( )
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法正确的是( )| A. | Mg电极是该电池的正极 | |
| B. | H2O2在石墨电极上发生氧化反应 | |
| C. | 石墨电极附近溶液的OH-的物质的量浓度增大 | |
| D. | 溶液中Cl-向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNH3和 1molHCl混合 | |
| B. | 1mol NO和 0.5 molO2混合 | |
| C. | 1molSO2和 1 molH2S混合 | |
| D. | 等体积的NO和NO2被足量烧碱溶液吸收 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4和C4H8 | B. | CH4和C3H6 | C. | C2H6和C3H6 | D. | C2H6和C4H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知六方氮化硼类似于石墨的结构,如图所示,利用所学知识结合该图回答下列问题.
已知六方氮化硼类似于石墨的结构,如图所示,利用所学知识结合该图回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com