
| A. | sp2杂化轨道形成σ键、未杂化的2p轨道形成π键 | |
| B. | sp2杂化轨道形成π键、未杂化的2p轨道形成σ键 | |
| C. | C、H之间形成的是s-p σ键,C、C之间的π键是未参加杂化的2p轨道形成的 | |
| D. | C、C之间形成的是sp2-sp2σ键,C、H之间是未参加杂化的2p轨道形成的π键 |
分析 A.杂化轨道用于填充孤对电子及成σ键;
B.杂化轨道用于填充孤对电子及成σ键;
C.乙烯中每个C原子形成2个C-H键、1个C=C双键,故杂化轨道数目为3,C原子采取sp2杂化,杂化轨道用于填充孤对电子及成σ键;
D.乙烯中每个C原子形成2个C-H键、1个C=C双键,故杂化轨道数目为3,C原子采取sp2杂化,杂化轨道用于填充孤对电子及成σ键.
解答 解:A.乙烯中sp2杂化轨道形成σ键,未杂化的2p轨道形成π键,故A正确;
B.乙烯中sp2杂化轨道形成σ键,未杂化的2p轨道形成π键,杂化轨道不能形成π键,故B错误;
C.乙烯中每个C原子成2个C-H键、1个C=C双键,故杂化轨道数目为2,C原子采取sp2杂化,杂化轨道用于填充孤对电子及成σ键,C-H之间是sp2杂化轨道形成σ键,C-C之间有未杂化的2p轨道形成的π键,故C错误;
D.乙烯中C原子成2个C-H键、1个C=C双键,故杂化轨道数目为2,C原子采取sp2杂化,杂化轨道用于填充孤对电子及成σ键,C-H之间是sp2杂化轨道形成σ键,C-C之间有未杂化的2p轨道形成的π键,故D错误;
故选A.
点评 本题考查了共价键的类型、杂化轨道、分子空间结构等,难度不大,注意杂化轨道用于填充孤对电子及成σ键.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 离子方程式 | 评价 |
| A | 将2 mol Cl2通入到含1 mol FeI2的溶液中: 2Fe2++2I-+2Cl2═2Fe3++4Cl-+I2 | 正确; Cl2过量,Fe2+、I-均被氧化 |
| B | 用Cu作电极电解NaCl溶液,阳极的电极反应式: 2Cl--2e-═Cl2↑ | 正确; Cl-优先于OH-放电 |
| C | 过量SO2通入到NaClO溶液中: SO2+H2O+ClO-═HClO+HSO | 正确; H2SO3的酸性强于HClO |
| D | Mg(HCO3)2溶液与足量的NaOH溶液反应: Mg2-+2HCO3-+4OH-═Mg(OH)2↓+2CO32-+2H2O | 正确; Mg(OH)2比MgCO3更难溶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | amol | B. | bmol | C. | (3a-b)mol | D. | (a+b)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸滴入NaAlO2溶液中 | B. | CO2气体通入漂白粉溶液中 | ||
| C. | NaOH溶液滴入AlCl3溶液中 | D. | Ba(OH)2溶液滴入Al2(SO4)3溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | K+ Ag+ Mg2+ Ba2+ |
| 阴离子 | NO3- CO32- SiO32- SO42- |
| 序号 | 实验内容 | 实验结果 |
| Ⅰ | 向该溶液中加入足量稀盐酸 | 产生白色沉淀并放出标准状况下0.56L气体 |
| Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
| Ⅲ | 向Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
| 阴离子 | NO3- | CO32- | SiO32- | SO42- |
| c(mol•h-1) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
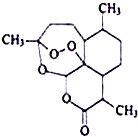 我国女药学家屠呦呦作为抗疟新药青蒿素的第一发明人荣获2015年诺贝尔生理学或医学奖.青蒿素的结构如图所示,下列关于青蒿素的说法错误的是( )
我国女药学家屠呦呦作为抗疟新药青蒿素的第一发明人荣获2015年诺贝尔生理学或医学奖.青蒿素的结构如图所示,下列关于青蒿素的说法错误的是( )| A. | 青蒿素的化学式为C15H22O5 | |
| B. | 青蒿素易溶于苯,难溶于水 | |
| C. | 青蒿素可与NaOH溶液发生水解反应 | |
| D. | 青蒿素的同分异构体不可能有芳香族化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径由大判小的顺序;Z>R>Y>W | |
| B. | X与Y形成化合物中一定含有离子键,可能含有共价键 | |
| C. | Y的氢化物比R的氢化物稳定,但Y的氢化物比R的氢化物熔沸点低 | |
| D. | RY2、WY2通入BaCl2溶液中均有白色沉淀生成. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com