
【题目】周期表前四周期的元素a、b、c、d、e,原子序数依次增大.a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子.回答下列问题:
(1)b、c、d中第一电离能最大的是______![]() 填元素符号
填元素符号![]() ,
,
(2)a和其他元素形成的二元共价化合物中,分子中既含有极性共价键、又含有非极性共价键的化合物是______![]() 填化学式,写出两种
填化学式,写出两种![]() .
.
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是______;酸根呈三角锥结构的酸是______![]() 填化学式
填化学式![]()
【答案】N ![]() 和
和![]()
![]() 、
、![]()
![]()
【解析】
周期表前四周期的元素a、b、c、d、e,原子序数依次增大,a的核外电子总数与其周期数相同,则a为H元素;
c的最外层电子数为其内层电子数的3倍,最外层电子数不超过8个,则c是O元素;
b的价电子层中的未成对电子有3个,且原子序数小于c,则b是N元素;
e的最外层只有1个电子,但次外层有18个电子,则e原子核外电子数为![]() ,为Cu元素;
,为Cu元素;
d与c同族,且原子序数小于e,所以d为S元素,据此进行解答。
(1)同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族和第VA族元素第一电离能大于其相邻元素,同一主族元素中,元素第一电离能随着原子序数增大而减小,所以b、c、d元素第一电离能最大的是N元素,
故答案为:N;
(2)a和其他元素形成的二元共价化合物中,既含有极性共价键、又含有非极性共价键的化合物有![]() 和
和![]() ,
,
故答案为:![]() 和
和![]() ;
;
(3)这些元素能够形成含氧酸的为N、S元素,N、S元素形成的含氧酸有![]() 、
、![]() 、
、![]() ,
,
![]() 中N原子价层电子对数是
中N原子价层电子对数是![]() ,含1对孤电子对,所以为V形结构,
,含1对孤电子对,所以为V形结构,
![]() 中N原子价层电子对数是
中N原子价层电子对数是![]() ,不含孤电子对,所以为平面三角形,
,不含孤电子对,所以为平面三角形,
![]() 中S原子价层电子对数是
中S原子价层电子对数是![]() ,含1对孤电子对,所以为三角锥形,
,含1对孤电子对,所以为三角锥形,
![]() 中S原子价层电子对数是
中S原子价层电子对数是![]() ,不含孤电子对,所以为正四面体,
,不含孤电子对,所以为正四面体,
则分子的中心原子的价层电子对数为3的酸是![]() 、
、![]() ;酸根呈三角锥结构的酸是
;酸根呈三角锥结构的酸是![]() ,
,
故答案为:![]() 、
、![]() ;
;![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有两种同分异构体。科学研究表明,两种分子都具有抗癌活性。
(1)吡啶分子是大体积平面配体,其结构简式如图所示![]() ,氮原子的杂化轨道方式是_____。吡啶分子中,各元素的电负性由大到小的顺序为_____。吡啶分子中含有_____个σ 键。
,氮原子的杂化轨道方式是_____。吡啶分子中,各元素的电负性由大到小的顺序为_____。吡啶分子中含有_____个σ 键。
(2)二氯二吡啶合铂分子中存在的微粒间作用力有_____(填序号)。
a.离子键 b.配位键 c.金属键 d.非极性键 e.氢键
(3)二氯二吡啶合铂分子中,Pt2+的配位数是 4,但是其轨道杂化方式并不是 sp3。简述理由:_____________。
(4)其中一种二氯二吡啶合铂分子结构如图所示,该分子是_____分子(选填“极性”、“非极性”)。
![]()
(5)CO(NH2)2 易溶于水的最主要原因是_________________________。
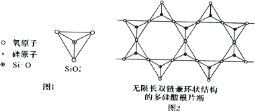
(6)Si 元素以 Si-O-Si 链构成矿物界,由许多四面体(图 l)连接成无限长的单链或双链(图 2)结构。图 2 所示的多硅酸根离子的化学式通式为_____(以含正整数n 的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g) ![]() Ni(CO)4(g),已知该反应平衡常数与温度的关系如表所示:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如表所示:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法正确的是( )
A. 上述生成Ni(CO)4(g)的反应为吸热反应
B. 25 ℃时反应Ni(CO)4(g) ![]() Ni(s)+4CO(g)的平衡常数为0.5
Ni(s)+4CO(g)的平衡常数为0.5
C. 在80 ℃时,测得某时刻,Ni(CO)4、CO浓度均0.5 mol/L,则此时v正>v逆
D. 80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中![]() 下列分析正确的是
下列分析正确的是![]()
![]()

A. ![]() 闭合,铁棒上发生的反应为
闭合,铁棒上发生的反应为![]()
B. ![]() 闭合,石墨棒周围溶液pH逐渐降低
闭合,石墨棒周围溶液pH逐渐降低
C. ![]() 闭合,铁棒不会被腐蚀,属于外加电流的阴极保护法
闭合,铁棒不会被腐蚀,属于外加电流的阴极保护法
D. ![]() 闭合,电路中通过
闭合,电路中通过![]() 个电子时,两极共产生
个电子时,两极共产生![]() 气体
气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基铁[Fe(CO)5]广泛用于催化剂,汽油抗爆剂,电子工业高频线圈制造。请回答下列问题:
(1)羰基铁[Fe(CO)5]中,碳、氧电负性大小比较____(用元素符号表示)。写出基态O的轨道表示式____;
(2)CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO分子中C原子的杂化类型为____杂化。
(3)1molFe(CO)5分子中含σ键数目为____;CO配体中的配位原子是____。
(4)科学家通过X射线探明,FeO、MgO、CaO的晶体结构与NaCl晶体结构相似,比较晶体熔点的高低MgO____CaO(填“高于”或“低于”)
(5)羰基铁[Fe(CO)5]中铁为0价。如图中的羰基铁为+3价,此羰基铁的晶体类型为____;此羰基铁中每个铁的配位数是____。
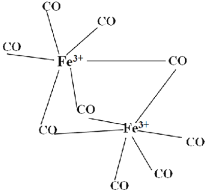
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下将NaOH溶液添加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是

A. Ka2(H2X)的数量级为10-6
B. 曲线N表示pH与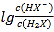 的变化关系
的变化关系
C. NaHX溶液中c(H+)>c(OH-)
D. 当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向50mL含有0.1molCl2的氯水中滴加2mol·L1的NaOH溶液,得到溶液pH随加入NaOH溶液体积的变化如图所示。下列说法正确的是
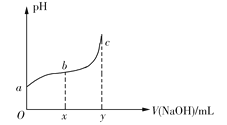
A.若a点pH=4,且c(Cl)=mc(HClO),则HClO的电离平衡常数为![]()
B.若x=100,b点对应溶液中,c(OH)>c(H+),可用pH试纸测定其pH
C.若y=200,c点对应溶液中,c(OH)c(H+)=2c(Cl)+c(HClO)
D.b→c段,随NaOH溶液的滴入,![]() 逐渐增大
逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中,水既不是氧化剂,也不是还原剂的是
A.2Na+2H2O=2NaOH+H2↑B.Cl2+H2O=HCl+HClO
C.2F2+2H2O=4HF+O2D.2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这种电池的电池反应式为:Li+2Li0.35NiO2![]() 2Li0.85NiO2,下列说法不正确的是( )
2Li0.85NiO2,下列说法不正确的是( )
A.放电时,负极的电极反应式:Li-e-=Li+
B.充电时,Li0.85NiO2既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质溶液
D.放电过程中Li+向负极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com