
×ī½üĆ½ĢåĘŲ¹ā³¬ŹŠ³öŹŪÓĆ¾ŪĀČŅŅĻ©ÖĘ³ÉµÄÓŠ¶¾±£ĻŹÄ¤£¬¾ŪĀČŅŅĻ©ĆܶȱČĖ®“󣬲»ĪČ¶Ø£¬³£³£¼ÓČė¼Ūøń½ĻµĶµÄÓ²Ö¬ĖįĒ¦×÷ĪČ¶Ø¼Į£¬Ņņ¶ų¶ŌČĖĢåÓŠŗ¦£¬¶ų¾ŪŅŅĻ©ĖÜĮĻĪŽ¶¾£¬ĆܶȱČĖ®Š””£ŅŌĻĀÓŠ¹Ų¾ŪŅŅĻ©ŗĶ¾ŪĀČŅŅĻ©µÄĖµ·ØÕżČ·µÄŹĒ £Ø””””£©”£
A£®¼ų±š¾ŪŅŅĻ©ŗĶ¾ŪĀČŅŅĻ©æɽ«ĖüĆĒ·Ö±š·ÅČėĖ®ÖŠ£¬ø”ŌŚĖ®ĆęÉĻµÄ ŹĒ¾ŪŅŅĻ©£¬³ĮŌŚĖ®ÖŠµÄŹĒ¾ŪĀČŅŅĻ©
B£®½«ĖüĆĒ·Ö±šµćČ¼£¬»šŃę¾ł·¢ŗŚ£¬Ć°ŗŚŃĢ£¬ÓŠ“Ģ±ĒµÄĘųĪ¶C£®¾ŪŅŅĻ©ŹōÓŚ¼Ó¾Ū²śĘ·£¬¾ŪĀČŅŅĻ©ŹōÓŚĖõ¾Ū²śĘ·
D£®¾ŪŅŅĻ©ŗĶ¾ŪĀČŅŅĻ©±£ĻŹÄ¤¶ŌČĖĢåĪ£ŗ¦²»“ó£¬æÉŅŌ·ÅŠÄŹ¹ÓĆ

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
C”¢NŹĒ¹¹³ÉÉśĆüÓŠ»śĢå±ŲŠčµÄŌŖĖŲ£¬Ęä»ÆŗĻĪļŌŚÉś»ī”¢Éś²śŗĶæĘѧъ¾æµČ·½Ćę¶¼ÓŠÖŲŅŖµÄÓ¦ÓĆ”£ŹŌ»Ų“šĻĀĮŠÓŠ¹ŲĪŹĢā£ŗ
(1)Ģ¼”¢µŖĮ½ŌŖĖŲµÄĒā»ÆĪļ·Šµć½ĻøߵďĒ____________,(Ģī»ÆѧŹ½)£¬ŌŅņŹĒ_________________________________________________________________”£
(2)Š“³öµŖŌŖĖŲµÄ»łĢ¬Ō×ӵĵē×ÓÅŲ¼Ķ¼£ŗ____________________________”£
(3)Ģ¼ŌŖĖŲÓėĒāŌŖĖŲŠĪ³ÉµÄĢžĄą»ÆŗĻĪļÖŠ£¬ÓŠŅ»Ąąŗ¬C”ŌCµÄČ²ĢžĄą»ÆŗĻĪļ£¬ČēŅŅČ²·Ö×ӵĽį¹¹¼ņŹ½ĪŖCH”ŌCH£¬Ęä·Ö×ÓÖŠŗ¬ÓŠ______øö¦Ņ¼ü£¬______øö¦Š¼ü£»ŅŃÖŖC”ŌCµÄ¼üÄÜĪŖ837 kJ”¤mol-1£¬C”ŖCµÄ¼üÄÜĪŖ347 kJ”¤mol-1£¬ŹŌ¼ĘĖćĖµĆ÷£¬CH”ŌCHŌŚ·¢Éś¼Ó³É·“Ó¦Ź±¶ĻĮѵďĒ______¼ü(Ģī”°¦Ņ”±»ņ”°¦Š”±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖĢģČ»ĘųµÄÖ÷ŅŖ³É·ÖCH4ŹĒŅ»ÖÖ»į²śÉśĪĀŹŅŠ§Ó¦µÄĘųĢ唣µČĪļÖŹµÄĮæµÄCH4ŗĶCO2²śÉśµÄĪĀŹŅŠ§Ó¦Ē°Õß“ó”£ĻĀĆęŹĒÓŠ¹ŲĢģČ»ĘųµÄ¼øÖÖŠšŹö£ŗ¢ŁĢģČ»ĘųÓėĆŗ”¢²ńÓĶĻą±ČŹĒ±Č½ĻĒå½ąµÄÄÜŌ“£»¢ŚµČÖŹĮæµÄCH4ŗĶCO2²śÉśµÄĪĀŹŅŠ§Ó¦Ņ²ŹĒĒ°Õß “󣻢ŪČ¼ÉÕĢģČ»Ęų£¬Ņ²ŹĒĖįÓźµÄ³ÉŅņÖ®Ņ»”£ĘäÖŠÕżČ·µÄŹĒ
“󣻢ŪČ¼ÉÕĢģČ»Ęų£¬Ņ²ŹĒĖįÓźµÄ³ÉŅņÖ®Ņ»”£ĘäÖŠÕżČ·µÄŹĒ
(””””)”£
A£®¢Ł¢Ś¢Ū B£®¢Ł
C£®¢Ł¢Ś D£®¢Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®HClOÖŠĀČŌŖĖŲ»ÆŗĻ¼Ū±ČHClO4ÖŠĀČŌŖĖŲ»ÆŗĻ¼ŪµĶ£¬ĖłŅŌ£¬HClO4µÄŃõ»ÆŠŌĒæ
B£®ŅŃÖŖ¢ŁFe + Cu2+ = Fe2+ + Cu£»¢Ś 2Fe3+ + Cu = 2Fe2+ + Cu2+£¬
ŌņŃõ»ÆŠŌĒæČõĖ³ŠņĪŖ£ŗFe3+ > Cu2£« > Fe2+
C£®ŅŃÖŖ»¹ŌŠŌ£ŗB£ > C£> D££¬·“Ó¦ 2C£ + D2 = 2D£ +C2ŗĶ
·“Ó¦ 2C£ + B2 = 2B£ +C2¶¼ÄÜ·¢Éś
D£®¾ßÓŠĒæŃõ»ÆŠŌŗĶĒ滹ŌŠŌµÄĪļÖŹ·ÅŌŚŅ»Ęš¾ĶÄÜ·¢ÉśŃõ»Æ»¹Ō·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŗø½ÓøÖĢśŹ±³£ÓƵÄŗøŅ©ĪŖĀČ»Æļ§£¬Ęä×÷ÓĆŹĒĻū³żŗø½Ó“¦µÄĢśŠā”£·¢ÉśµÄ·“Ó¦ĢåĻµÖŠ¹²ÓŠĮłÖÖĪļÖŹ£ŗNH4C1”¢FeC13”¢N2”¢Fe2O3”¢FeŗĶX”£
£Ø1£©øł¾ŻĢāŅā£¬æÉÅŠ¶Ļ³öXŹĒ £ØŠ“»ÆѧŹ½£©”£
£Ø2£©Š“³ö²¢ÅäĘ½øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ ”£
£Ø3£©·¢ÉśŃõ»Æ·“Ó¦µÄĪļÖŹŹĒ £¬·“Ó¦ÖŠ4molµÄŃõ»Æ¼ĮÄÜ £ØĢī”°Ź§Č„”±»ņ”°µĆµ½”±£© molµē×Ó.
£Ø4£©·“Ó¦ÖŠ±»Ńõ»Æ²śÉśĮĖ11.2L£Ø±ź×¼×“æö£©µÄĘųĢåŹ±£¬±»»¹ŌµÄĪļÖŹµÄÖŹĮæĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓŠ¹Ų½šøÕŹÆµÄĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £Ø””””£©”£
A£®½šøÕŹÆŹĒŌ×Ó¾§Ģ壬¹¹³ÉĪ¢Į£ŹĒŌ×Ó
B£®½šøÕŹÆ»ÆѧŠŌÖŹŗÜĪČ¶Ø£¬²»ČÜÓŚĖ®£¬ÄĶĖį¼īøÆŹ“
C£®½šøÕŹÆµÄČŪµć±Č½šøÕÉ°µÄČŪµćµĶ
D£®½šøÕŹÆ¾§ĢåÖŠĢ¼Ō×ÓŠĪ³ÉµÄ»·ÖŠ£¬×īŠ”µÄ»·ŗ¬ÓŠ4øöĢ¼Ō×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
±ūĶéµÄ·Ö×Ó½į¹¹æɼņŠ“³É¼üĻߏ½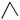 £¬ÓŠ»śĪļAµÄ¼üĻߏ½½į¹¹ĪŖ
£¬ÓŠ»śĪļAµÄ¼üĻߏ½½į¹¹ĪŖ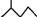 £¬ÓŠ»śĪļBÓėµČĪļÖŹµÄĮæµÄH2·¢Éś¼Ó³É·“Ó¦æɵƵ½ÓŠ»śĪļA”£ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
£¬ÓŠ»śĪļBÓėµČĪļÖŹµÄĮæµÄH2·¢Éś¼Ó³É·“Ó¦æɵƵ½ÓŠ»śĪļA”£ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
A£®ÓĆĻµĶ³ĆüĆū·ØĆüĆūÓŠ»śĪļA£¬Ćū³ĘĪŖ2-¼×»łĪģĶé
B£®ÓŠ»śĪļAµÄŅ»ĀČČ”“śĪļÓŠ4ÖÖ
C£®ÓŠ»śĪļAµÄ·Ö×ÓŹ½ĪŖC6H14
D£®BµÄ½į¹¹æÉÄÜÓŠ4ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ē¦Šīµē³ŲµÄ¹¤×÷ŌĄķĪŖ£ŗPb£«PbO2£«2H2SO4===2PbSO4£«2H2O”£ŃŠ¶ĮĻĀĶ¼£¬ĻĀĮŠÅŠ¶Ļ²»ÕżČ·µÄŹĒ(””””)
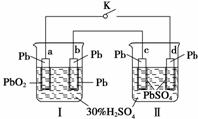
A£®K±ÕŗĻŹ±£¬dµē¼«·“Ó¦Ź½£ŗPbSO4£«2H2O”Ŗ”śPbO2£«4H£«£«SO £«2e£
£«2e£
B£®µ±µēĀ·ÖŠ×ŖŅĘ0.2 molµē×ÓŹ±£¬¢ńÖŠĻūŗĵÄH2SO4ĪŖ0.2 mol
C£®K±ÕŗĻŹ±£¬¢ņÖŠSO Ļņcµē¼«ĒØŅĘ
Ļņcµē¼«ĒØŅĘ
D£®K±ÕŗĻŅ»¶ĪŹ±¼äŗ󣬢ņæɵ„¶Ą×÷ĪŖŌµē³Ų£¬dµē¼«ĪŖÕż¼«
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com