
”¾ĢāÄæ”æNH3ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬ŌŚÉś²ś”¢Éś»īÖŠÓĆĶ¾¹ć·ŗ”£
£Ø1£©ŅŃÖŖ£ŗ
¹²¼Ū¼ü | ¼üÄÜ/ kJ”¤mol-1 |
HØDH | 436 |
N”ŌN | 946 |
NØDH | 391 |
×¢£ŗ²šæŖĘųĢ¬ĪļÖŹÖŠ1 molijÖÖ¹²¼Ū¼üŠčŅŖĪüŹÕµÄÄÜĮ棬¾ĶŹĒøĆ¹²¼Ū¼üµÄ¼üÄÜ”£
N2 (g)£«3 H2 (g)![]() 2 NH3 (g) H =____kJ”¤mol-1
2 NH3 (g) H =____kJ”¤mol-1
£Ø2£©Ņ»¶ØĪĀ¶ČĻĀ£¬ĻņŗćČŻµÄĆܱÕČŻĘ÷ÖŠ³äČėN2ŗĶH2·¢Éś·“Ó¦£ŗN2 £«3H2 ![]() 2NH3£¬²āµĆø÷×é·ÖÅضČĖꏱ¼ä±ä»ÆČēĶ¼1ĖłŹ¾”£
2NH3£¬²āµĆø÷×é·ÖÅضČĖꏱ¼ä±ä»ÆČēĶ¼1ĖłŹ¾”£
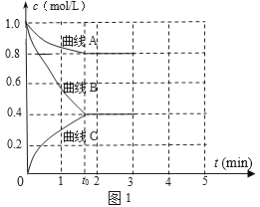
¢Ł±ķŹ¾c(N2)µÄĒśĻߏĒ__£ØĢī”°ĒśĻßA”±”¢”°ĒśĻßB”±»ņ”°ĒśĻßC”±£©”£
¢Ś0”«t0Ź±ÓĆH2±ķŹ¾·“Ó¦ĖŁĀŹv(H2)____mol”¤L-1”¤min-1”£
¢ŪĻĀĮŠÄÜĖµĆ÷øĆ·“Ó¦“ļµ½Ę½ŗāµÄŹĒ____”£
a£®»ģŗĻĘųĢåµÄŃ¹Ēæ²»ŌŁ±ä»Æ
b£®2c(H2)= 3c(NH3)
c£®»ģŗĻĘųĢåµÄÖŹĮæ²»ŌŁ±ä»Æ
d£®NH3µÄĢå»ż·ÖŹż²»ŌŁ±ä»Æ
£Ø3£©Ē±Ķ§ÖŠŹ¹ÓƵÄŅŗ°±-ŅŗŃõČ¼ĮĻµē³Ų¹¤×÷ŌĄķČēĶ¼2ĖłŹ¾£ŗ
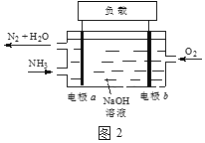
¢Łµē¼«bĆū³ĘŹĒ____”£
¢Śµē½āÖŹČÜŅŗÖŠOH-Ąė×ÓĻņ____ŅĘ¶Æ£ØĢī”°µē¼«a”±»ņ”°µē¼«b”±£©”£
¢Ūµē¼«aµÄµē¼«·“Ó¦Ź½ĪŖ____”£
£Ø4£©æÉĶعżNH3ÓėNaClO·“Ó¦Ą“Öʵƻš¼żČ¼ĮĻėĀ£ØN2H4£©”£øĆ·“Ó¦µÄ»Æѧ·“Ó¦·½³ĢŹ½ŹĒ____”£
”¾“š°ø”æ -92 ĒśĻßA 0.6/t0 a d Õż¼« µē¼«a 2NH3 + 6OH££6e£ = N2 + 6H2O 2NH3 + NaClO = N2H4+ NaCl + H2O
”¾½āĪö”æ(1)·“Ó¦ČȵÄģŹ±ä”÷H=·“Ó¦Īļ×ܼüÄÜ-Éś³ÉĪļ×ܼüÄÜ£¬N2 (g)£«3 H2 (g)![]() 2 NH3 (g) H =436”Į3+946”Į1-391”Į6=-92kJ”¤mol-1£¬¹Ź“š°øĪŖ£ŗ-92£»
2 NH3 (g) H =436”Į3+946”Į1-391”Į6=-92kJ”¤mol-1£¬¹Ź“š°øĪŖ£ŗ-92£»
(2)¢ŁŌŚŗćČŻµÄĆܱÕČŻĘ÷ÖŠ³äČėN2ŗĶH2·¢Éś·“Ó¦£ŗN2 £«3H2 ![]() 2NH3£¬Ėę×Å·“Ó¦µÄ½ųŠŠ£¬µŖĘųµÄÅضČÖš½„¼õŠ”£¬¼õŠ”·ł¶Č±ČĒāĘųŠ”£¬Ņņ“Ė±ķŹ¾c(N2)µÄĒśĻߏĒĒśĻßA£¬¹Ź“š°øĪŖ£ŗĒśĻßA£»
2NH3£¬Ėę×Å·“Ó¦µÄ½ųŠŠ£¬µŖĘųµÄÅضČÖš½„¼õŠ”£¬¼õŠ”·ł¶Č±ČĒāĘųŠ”£¬Ņņ“Ė±ķŹ¾c(N2)µÄĒśĻߏĒĒśĻßA£¬¹Ź“š°øĪŖ£ŗĒśĻßA£»
¢Ś0”«t0Ź±ÓĆH2±ķŹ¾·“Ó¦ĖŁĀŹv(H2)=![]() =
= ![]() mol”¤L-1”¤min-1£¬¹Ź“š°øĪŖ£ŗ
mol”¤L-1”¤min-1£¬¹Ź“š°øĪŖ£ŗ![]() £»
£»
¢Ūa£®ŗćČŻµÄĆܱÕČŻĘ÷£¬Ń¹ĒæÖš½„¼õŠ”£¬»ģŗĻĘųĢåµÄŃ¹Ēæ²»ŌŁ±ä»Æ£¬ÄÜĖµĆ÷“ļµ½Ę½ŗā£¬ÕżČ·£»b£®2c(H2)= 3c(NH3)²»ÄÜĖµĆ÷ÅØ¶ČŹĒ·ń±ä»Æ£¬Ņņ“Ė²»ÄÜĖµĆ÷“ļµ½Ę½ŗā£¬“ķĪó£»c£®øł¾ŻÖŹĮæŹŲŗć¶ØĀÉ£¬»ģŗĻĘųĢåµÄÖŹĮæŹ¼ÖÕ²»±ä£¬²»ÄÜĖµĆ÷“ļµ½Ę½ŗā£¬“ķĪó£»d£®NH3µÄĢå»ż·ÖŹż²»ŌŁ±ä»Æ£¬ĖµĆ÷ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬ÄÜĖµĆ÷“ļµ½Ę½ŗā£¬ÕżČ·£»¹ŹŃ”ad£»
(3)¢ŁŌŚČ¼ĮĻµē³ŲÖŠĶØČėČ¼ĮĻµÄĪŖøŗ¼«£¬ŃõĘųµÄĪŖÕż¼«£¬Ōņµē¼«aĪŖøŗ¼«£¬µē¼«bĪŖÕż¼«£¬¹Ź“š°øĪŖ£ŗÕż¼«£»
¢ŚŌŚČ¼ĮĻµē³ŲÖŠµē½āÖŹČÜŅŗÖŠOH-Ąė×ÓĻņµē¼«aŅĘ¶Æ£¬¹Ź“š°øĪŖ£ŗµē¼«a£»
¢ŪŌŚČ¼ĮĻµē³ŲµÄøŗ¼«ÉĻ·¢ÉśČ¼ĮĻ°±ĘųŹ§µē×ÓµÄŃõ»Æ·“Ó¦£¬Ōņ¼īŠŌ»·¾³ĻĀµē¼«aĪŖøŗ¼«£¬·¢ÉśµÄµē¼«·“Ó¦ĪŖ£ŗ2NH3+6OH--6e-=N2”ü+6H2O¹Ź“š°øĪŖ£ŗ2NH3+6OH--6e-ØTN2+6H2O”£
(4)NH3ÓėNaClO·“Ó¦Ą“Öʵƻš¼żČ¼ĮĻėĀ(N2H4)£¬·“Ó¦µÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ2NH3 + NaClO = N2H4+ NaCl + H2O£¬¹Ź“š°øĪŖ£ŗ2NH3 + NaClO = N2H4+ NaCl + H2O”£


 ĮéŠĒ¼ĘĖ抔“ļČĖĻµĮŠ“š°ø
ĮéŠĒ¼ĘĖ抔“ļČĖĻµĮŠ“š°ø ĆĻ½ØĘ½“ķĢā±¾ĻµĮŠ“š°ø
ĆĻ½ØĘ½“ķĢā±¾ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·ūŗÅĪŖKµÄÄܲć×ī¶ąÄÜČŻÄɵĵē×ÓŹżĪŖ(””””)
A. 2B. 32
C. 50D. 72
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷ĪļÖŹÖŠ£¬²»ÄÜ·¢ÉśĖ®½ā·“Ó¦µÄŹĒ£Ø £©
A.ĘĻĢŃĢĒ
B.ĻĖĪ¬ĖŲ
C.ÓĶÖ¬
D.Ćø
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£Źż£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
A.32g O2ĘųĢåŗ¬ÓŠµÄŃõŌ×ÓŹżĪŖNA
B.2L 0.3mol/L Na2SO4ČÜŅŗÖŠŗ¬ÓŠNa£«ĪŖ0.6NA
C.27gĀĮĶźČ«·“Ó¦ŗóŹ§Č„µÄµē×ÓŹżĪŖ3NA
D.11.2LµŖĘųĖłŗ¬µÄ·Ö×ÓŹżĪŖ0.5NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷Ō×Ó»ņĄė×ӵĵē×ÓÅŲ¼Ź½“ķĪóµÄŹĒ £Ø £©
A. Na+£ŗ 1s22s22p6 B. F £ŗ1s22s22p5
C. O2”Ŗ£ŗ 1s22s22p4 D. Ar£ŗ 1s22s22p63s23p6
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij¹¤³§×ŪŗĻ“¦Ąķŗ¬![]() ·ĻĖ®ŗĶ¹¤Ņµ·ĻĘų£ØÖ÷ŅŖŗ¬N2”¢CO2”¢SO2”¢NO”¢CO£¬²»æ¼ĀĒĘäĖū³É·Ö£©£¬Į÷³ĢČēĶ¼ĖłŹ¾£ŗ
·ĻĖ®ŗĶ¹¤Ņµ·ĻĘų£ØÖ÷ŅŖŗ¬N2”¢CO2”¢SO2”¢NO”¢CO£¬²»æ¼ĀĒĘäĖū³É·Ö£©£¬Į÷³ĢČēĶ¼ĖłŹ¾£ŗ

£Ø1£©¹ĢĢå1µÄÖ÷ŅŖ³É·Ö³żCa(OH)2Ķā£¬»¹ÓŠ____”¢____£ØĢī»ÆѧŹ½£©”£
£Ø2£©ĪŖŹ¹·“Ó¦¢ŁÖŠµÄÓŠ¹ŲĘųĢå±»³ä·ÖĪüŹÕ£¬æɲÉČ”µÄ“ėŹ©ÓŠ£ŗ¢ŁŌö“ó½Ó“„Ć껿£»¢Ś____”£
£Ø3£©ŅŃÖŖ£ŗ
2NO2+2NaOH=NaNO3+NaNO2+H2O
NO2+NO+2NaOH=2NaNO2+H2O
ĪŖČ·±£·“Ó¦¢Ūֻɜ³ÉNaNO2£¬ĄķĀŪÉĻÓ¦æŲÖĘNOÓėO2µÄĪļÖŹµÄĮæÖ®±ČĪŖ____£»“ĖŹ±·“Ó¦¢ÜµÄĄė×Ó·½³ĢŹ½ĪŖ____”£Čōn(NO) :n(O2)=3:1£¬ĒŅNaOHČÜŅŗ×ćĮ棬ŌņĖłµĆČÜŅŗ1ÖŠNaNO3ÓėNaNO2µÄĪļÖŹµÄĮæÖ®±ČĪŖ____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹ¼ČÄÜÓėŃĪĖį·“Ó¦ÓÖÄÜÓėNaOHČÜŅŗ·“Ó¦£¬²¢ĒŅ¶¼·Å³öĒāĘųµÄŹĒ
A. Fe B. Al C. Al2O3 D. Si
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹŹōÓŚĄė×Ó»ÆŗĻĪļµÄŹĒ£Ø £©
A.HCl
B.NH3H2O
C.£ØNH4£©2SO4
D.CH3COOH
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķŹĒŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö,±ķÖŠĖłĮŠµÄ×ÖÄø·Ö±š“ś±ķijŅ»»ÆѧŌŖĖŲ”£
A | ||||||||
B | C | |||||||
D | E | F | ||||||
»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ŌŖĖŲBµÄŌŖĖŲ·ūŗÅĪŖ______£¬ĖüŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ__________”£
(2)DµÄ¼ņµ„Ąė×ӵĽį¹¹Ź¾ŅāĶ¼ĪŖ_________£¬ĖüµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļÖŠŗ¬ÓŠµÄ»Æѧ¼üÓŠ_____________£¬Dµ„ÖŹÓėĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ____________________”£
(3)ÓƵē×ÓŹ½±ķŹ¾EF2µÄŠĪ³É¹ż³Ģ_________________________________”£
(4)ÓÉA2”¢C2¹¹³É¼īŠŌČ¼ĮĻµē³Ų£¬ŌņøƵē³ŲµÄøŗ¼«·“Ó¦·½³ĢŹ½ĪŖ_______________£¬øƵē³Ų¹¤×÷¹ż³ĢÖŠĆæĶعż2molµē×ÓĖłŠčŅŖµÄC2Ģå»żĪŖ___________(±ź×¼×“æö)”£
(5)CŗĶDŌŚøßĪĀĢõ¼žĻĀŠĪ³É»ÆŗĻĪļµÄ»ÆѧŹ½ĪŖ_________£¬Óė¶žŃõ»ÆĢ¼·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_________________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com