
下列有关金属腐蚀与保护的说法正确的是
A.钢铁在潮湿空气中发生吸氧腐蚀,负极反应为Fe-3e-===Fe3+
B.相同条件下,轮船在海水中比在淡水中腐蚀慢
C.铁上镀锌的保护方法叫牺牲负极的正极保护法
D.水库里钢闸门与电源负极相连的方法叫做外加电流的阴极保护法
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源:2014-2015山东省临沂市高一上学期期期末统考化学试卷(解析版) 题型:选择题
设阿伏加德罗常数的数值为,下列叙述正确的是
A.标准状况下,22.4L四氯化碳含有的分子数为
B.1 mol硫酸钾中阴离子所带的电荷数为2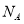
C.0.5 mol NaOH溶液中 Na+数为0.5
NaOH溶液中 Na+数为0.5
D.常温常压下,16g氧气所含电子数为
查看答案和解析>>
科目:高中化学 来源:2014-2015宁夏回族自治区银川一中高一上学期期末考试化学试卷(解析版) 题型:选择题
在A、B两烧杯溶液中,含有Fe2+、Na+、H+、NO3—、Cl—、OH—6种离子。已知B烧杯的溶液无色(含有其中三种离子),则A烧杯的溶液中大量存在的离子是
A.NO3—、OH—、Cl— B.Fe2+、H+、Cl—
C.Fe2+、OH—、NO3— D.Na+、H+、OH—
查看答案和解析>>
科目:高中化学 来源:2014-2015宁夏回族自治区银川一中高二上学期期末考试化学试卷(解析版) 题型:选择题
1L 0.1mol/L的AgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极上增重2.16g时,下列判断正确的是
A.电解质AgNO3溶液的浓度变为0.08mol/L
B.阳极上产生112mLO2(标况)
C.转移1.204×1022个电子
D.反应中有0.01mol的Ag被氧化
查看答案和解析>>
科目:高中化学 来源:2014-2015宁夏回族自治区银川一中高二上学期期末考试化学试卷(解析版) 题型:选择题
25℃时,向纯水中加入NaOH,使溶液的pH为11,则该溶液中由NaOH电离出的c(OH-)与由水电离出的c(OH-)之比为
A.108∶1 B.5×109∶1 C.1010∶1 D.1∶1
查看答案和解析>>
科目:高中化学 来源:2014-2015宁夏回族自治区银川一中高二上学期期末考试化学试卷(解析版) 题型:选择题
将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。已知,通入 CH4的一极,其电极反应式是CH4+10OH--8e-===CO32-+7H2O;通入O2的另一极,其电极反应式是2O2+4H2O+8e-===8OH-。下列叙述不正确的是
A.正极发生还原反应
B.通入CH4的电极为负极
C.该电池使用一段时间后应补充KOH
D.燃料电池工作时,溶液中的OH-向正极移动
查看答案和解析>>
科目:高中化学 来源:2014-2015辽宁省大连市高一上学期期末考试化学试卷(解析版) 题型:填空题
(11分)某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题:

(1)请写出Fe2O3与①反应的离子方程式______________________________。
(2)物质②为_______________。
(3)请写出FeCl3与铁粉反应的化学方程式________________________。
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为_________,此过程中发生的氧化还原反应为(用化学方程式表达)_________________________。
(5)将FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得分散系③__________________,它与FeCl3溶液、Fe(OH)3浊液的本质区别是_________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015辽宁省大连市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.生铁、不锈钢和黄铜都属于合金
B.水泥、玻璃、陶瓷均属于无机非金属材料
C.氧化钙、氧化镁、氧化铝都属于碱性氧化物
D.溶液、胶体、浊液都属于分散系
查看答案和解析>>
科目:高中化学 来源:2014-2015辽宁省大连市高二上学期期末考试化学(理)试卷(解析版) 题型:选择题
某学习小组用锌片、铜片和稀硫酸进行原电池的相关探究,下列说法正确的是
A.溶液的pH增大
B.溶液中的H+向锌电极定向移动
C.锌电极的反应为2H+ + 2e- = H2 ↑
D.外电路中,电子由铜电极转移到锌电极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com