
【题目】设NA表示阿伏加德罗常数的值,下列有关叙述正确的有( )
①标准状况下,20 g 重水(D2O)中含有的电子数为 10NA
②0.5 molFe2+被足量的 H2O2 溶液氧化,转移 0.5NA个电子
③将 2 mol NO 和 1 mol O2 混合后,体系中的分子总数为 3NA
④乙烯和环丙烷组成的 42 g 混合气体中氢原子的个数为 6NA
⑤2 molL﹣1 碳酸钠溶液中 Na+的数目是 2NA
⑥10LpH=1 的硫酸溶液中含有的 H+数为 2NA
⑦22.4 L 的 N2 的共用电子对数为 3NA
⑧将 0.1mol 氯化铁溶于 1L 水中,所得溶液含有 NA0.1个 Fe3+.
A.①④⑥ B.②③④ C.①②④ D.①②④⑧
【答案】C
【解析】①20g重水(D2O)的物质的量是1mol,D2O分子中含有10个电子,含有的电子数为10NA,故①正确;
②0.5 molFe2+被足量的 H2O2 溶液氧化生成0.5mol三价铁离子,转移 0.5NA个电子,故②正确;
③2mol NO和1molO2混合后生成了1mol二氧化氮,体系中的分子总数小于3NA,故③错误;
④乙烯和环丙烷最简式相同为CH2,计算42gCH2中氢原子数=![]() ×2×NA=6NA,故④正确;
×2×NA=6NA,故④正确;
⑤溶液体积未知,无法计算钠离子个数,故⑤错误;
⑥10L pH=1的硫酸溶液中氢离子浓度为0.1mol/L,1L溶液中含有0.1mol氢离子,含有的H+离子数为NA,故⑥错误;
⑦气体状况未知,无法计算氮气的物质的量,无法计算N2 的共用电子对数,故⑦错误;
⑧Fe3+在溶液中发生水解,Fe3+的物质的量小于0.1mol,所以溶液含有Fe3+数目小于0.1NA个,故⑧错误。


科目:高中化学 来源: 题型:
【题目】CH4和H2O在一定条件下, 可以转化为合成一系列有机化合物、氨的重要原料(CO+H2),这种方法称作甲烷水蒸气重整法制合成气,其能量变化如图:

(1)甲烷水蒸气重整法制合成气的热化学方程式为_______;该反应只有在_____(填“高温”、“低温”或“常温”)才自发进行。
(2)下列有关甲烷水然气重整法制合成气的说法正确的是_____(填字母)。
A.相同条件下,该反应的逆反应更易发生
B.恒温恒容时充入一定量CO2,可促进CH4转化并可调节CO和H2的比例
C.若反应的高效催化剂为A,则A一定是CO和H2合成CH4的高效催化剂
D.恒温时向上述平衡体系中充入少量Ar,平衡一定不移动
E.有副反应:H2O+CO![]() CO2+H2
CO2+H2
(3)在恒容密闭容器中充入2mol的CH4和H2O(g)混合气体,且CH4和H2O(g)的物质的量之比为x,相同温度下测得H2平衡产率与x的关系如图所示。请问a、b两点比较(填“>”、“<”、“=”);CH4的转化率a点____b点,a点CH4的浓度_____b点H2O(g)的浓度,氢气的产率a点_____b点。

(4)当充入CH4和H2O(g)物质的量之比1:2.2时,温度、压强p对平衡时CO体积分数φ(CO)的影响如图,则压强由大到小的排序是_____;当T<450℃和T≥1000℃时,压强p对φ(CO)几乎无影响的原因是_____________________。

(5)在下图左室充入1molCH4和H2O(g)混合气体(物质的量之比为1:1),恒温条件下反应建立平衡,测得CH4的转化率为50%,则其平衡常数为_________ 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施或事实不能用勒沙特列原理解释的是 ( )
A.滴加酚酞的氨水中加入氯化铵固体后红色变浅
B.棕红色的NO2加压后颜色先变深后变浅(已知: 2NO2 (g) ![]() N2O4 (g))
N2O4 (g))
C.工业上生产硫酸的过程中,使用过量的空气以提高SO2的利用率
D.用硫酸氢钠去除暖水瓶中的水垢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.硅元素在自然界里均以化合态存在
B.SiO2不能与水反应生成硅酸,不是酸性氧化物
C.除去二氧化硅中少量的碳酸钙杂质应选用水
D.粗硅制备时,发生的反应为C+SiO2=Si+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1;元素Y基态原子的3p轨道上有5个电子;元素Z的原子最外层电子数是其内层电子数的3倍;元素W基态原子的核外电子共有16种运动状态。
(1)①在元素周期表中,元素X位于 区,元素Y在周期表中的位置是 。
②Z所在周期中,第一电离能最大的元素是 (填元素名称)。
③X+的核外电子排布式为 。
④Y和W两元素最高价氧化物对应的水化物酸性较强的是 (填化学式)。
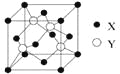
(2)X与Y所形成化合物晶体的晶胞如右图所示。在1个晶胞中,X离子的数目为 ;该化合物的化学式为 。
(3)①在乙醇中的溶解度:Z的氢化物(H2Z)大于H2W,其主要原因是 。
②稳定性:H2Z H2W(填“>”、“<”或“=”),其主要原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列固体混合物与过量的稀H2SO4反应,能产生气泡并有沉淀生产的是( )
A.NaHCO3和Al(OH)3
B.BaCl2和NaCl
C.KClO3和K2SO4
D.Na2SO3和BaCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com