
 已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题: (1)X元素原子基态时的电子排布式为
(1)X元素原子基态时的电子排布式为 
 ,该元素的符号是__________;
,该元素的符号是__________; (2)Y元素原子的价层电子的轨道表示式为
(2)Y元素原子的价层电子的轨道表示式为 
 ,该元素的名称是___
,该元素的名称是___ _______;
_______; (3)X与Z可形成化合物XZ3,该化合物的空间构型为____________; X原子的杂化轨道类型为_______
(3)X与Z可形成化合物XZ3,该化合物的空间构型为____________; X原子的杂化轨道类型为_______ (4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是_________________________________________________;
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是_________________________________________________; (5)比较X的氢化物与同族第二、第三周期元素所形成
(5)比较X的氢化物与同族第二、第三周期元素所形成 的氢化物沸点高低顺序为
的氢化物沸点高低顺序为 
 。
。科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 其氢化物反应生成一种盐Y,A、B、C、E、F五种元素都能与D元素形成原子个数比不相同的常见化合物。回答下列问题:
其氢化物反应生成一种盐Y,A、B、C、E、F五种元素都能与D元素形成原子个数比不相同的常见化合物。回答下列问题: 充分作用后,溶液pH 7(填“>”“<”或“=”),原因是
充分作用后,溶液pH 7(填“>”“<”或“=”),原因是  。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
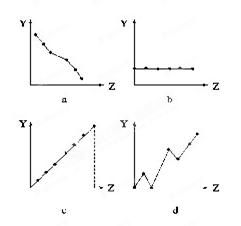
 元素有关的性质相符的曲线标号填入相应的空格中:
元素有关的性质相符的曲线标号填入相应的空格中:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。请回答:
况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。请回答:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深 |
| B.氧族元素氢化物稳定性按H2O、H2S、H2Se、H2Te的顺序依次减小 |
| C.氢化物的沸点按NH3、BiH3、SbH3、AsH3、PH3的顺序依次递减 |
| D.最高价氧化物对应水化物碱性按NaOH、KOH、RbOH、CsOH的顺序依次增强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 不正确的是
不正确的是| A.沸点:HF>HCl>HBr | B.熔点:I2>H2O>H2S |
| C.酸性:HClO4>H2SO4>H2CO3 | D.离子半径:S2->F->Na+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.16、16、16 | B.18、16、16 | C.18、18、16 | D.16、16、18 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com