
| 1+x |
| 1-x |
| 2 |
| 1 |
| 1 |
| 3 |
| 1 |
| 3 |


科目:高中化学 来源: 题型:
| 点燃 |
| 高温 |
| 高温 |
| A、②③ | B、①④ |
| C、②③④ | D、只有② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用FeCl3溶液腐蚀印刷电路板上铜箔:2Fe3++Cu=2Fe2++Cu2+ |
| B、Fe与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| C、氢氧化钡溶液与硫酸反应:Ba2++SO42-+OH-+H+=H2O+BaSO4↓ |
| D、向小苏打溶液中滴入醋酸:CO32-+2CH3COOH=CO2↑+H2O+2CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
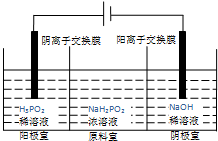 磷有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常为化工生产中的还原剂.
磷有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常为化工生产中的还原剂.查看答案和解析>>
科目:高中化学 来源: 题型:
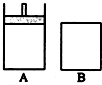 A容器是能 保持恒压的密闭容器,有一个能移动的活塞.B容器是保持恒容的密闭容器(如图所示),开始时,向A和B容器中分别充入2mol SO2 与1mol O2的混合气体,并且使A与B的容积相等,在一定温度下反应:2SO2(g)+O2(g)?2SO3(g)+Q(Q>0).
A容器是能 保持恒压的密闭容器,有一个能移动的活塞.B容器是保持恒容的密闭容器(如图所示),开始时,向A和B容器中分别充入2mol SO2 与1mol O2的混合气体,并且使A与B的容积相等,在一定温度下反应:2SO2(g)+O2(g)?2SO3(g)+Q(Q>0).查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
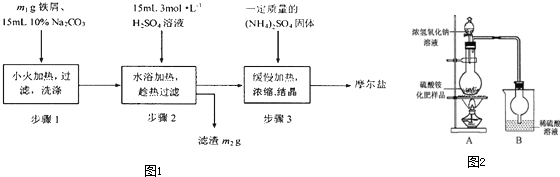
| 指标 项目 | 优等品 | 一等品 | 合格品 |
| 外观 | 白色结晶,无可见机械杂质 | 无可见机械杂质 | |
| 氮(N) | ≥21.0% | ≥21.0% | ≥20.5% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com