
【题目】a mol FeS与b mol FeO投入到V L c mol/L的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看做是Fe(NO3)3、H2SO4的混合液,则在反应中未被还原的硝酸可能为
① (![]() )mol ②(a+b)×189 g ③(3a+3b)mol ④
)mol ②(a+b)×189 g ③(3a+3b)mol ④![]() mol
mol
A. ②④ B. ②③ C. ①②③ D. ②③④
【答案】D
【解析】当硝酸恰好反应时,生成硝酸铁的硝酸就是未被还原的硝酸,由元素守恒知:未被还原的硝酸将转化为Fe(NO3)3中的NO3 -,所以显酸性的硝酸的物质的量等于Fe(NO3)3的物质的量的3倍,由元素守恒知,n〔Fe(NO3)3〕=n(Fe)=(a+b)mol,所以未被还原的硝酸的物质的量为3(a+b)mol,未被还原的硝酸的质量=3(a+b)mol×63 gmol-1=(a+b)×189 g,故②③正确;当硝酸过量时,除去生成一氧化氮的硝酸就是未被还原的硝酸,反应中Fe元素由+2升高为+3,硫元素由-2升高为+6,氮元素由+5降低为+2,根据电子转移降守恒知:n(NO)=![]() =
=![]() mol,即显氧化性的硝酸的物质的量=
mol,即显氧化性的硝酸的物质的量=![]() mol,所以未被还原的硝酸为[Vc-
mol,所以未被还原的硝酸为[Vc-![]() ]mol,故④正确,故答案为D。
]mol,故④正确,故答案为D。


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】准确量取25.00mLKMnO4溶液,可选用的仪器是( )
A.25mL量筒B.25mL酸式滴定管
C.25mL碱式滴定管D.有刻度的50mL烧杯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组在实验室以含铁的铜屑为原料制备Cu(NO3)23H2O晶体,并进一步探究用SOCl2制备少量无水Cu(NO3)2.设计的合成路线如下:
已知:①Cu(NO3)23H2O![]() Cu(NO3)2Cu(OH)2
Cu(NO3)2Cu(OH)2![]() CuO
CuO
②SOCl2熔点﹣105℃、沸点76℃、遇水剧烈水解生成两种酸性气体、水解强烈放热,
请回答:
(1)Cu与足量稀HNO3反应的化学方程式_____
(2)第②步调pH适合的物质是_____(填化学式).
(3)第③步包括蒸发浓缩、冷却结晶、过滤等步骤,其中蒸发浓缩的具体操作是_____.为得到较大颗粒的Cu(NO3)23H2O晶体,可采用的方法是_____(填一种).
(4)第④步中发生的反应化学方程式是_____.
(5)第④步,某同学设计的实验装置示意图(如图1)有一处不合理,请提出改进方案并说明理由:_____;装置改进后,向仪器A中缓慢滴加SOCl2时,需打开活塞_____(填“a”、“b”或“a和b”).反应过程中,可能会因温度过高而有副反应,写出两种有效措施_____、_____.
(6)为测定无水Cu(NO3)2产品的纯度,可用分光光度法.
已知:4NH3H2O+Cu2+═Cu(NH3)42++4H2O;Cu(NH3)42+对特定波长光的吸收程度(用吸光度A表示)与Cu2+在一定浓度范围内成正比.现测得Cu(NH3)42+的吸光度A与Cu2+标准溶液浓度关系如图2所示:
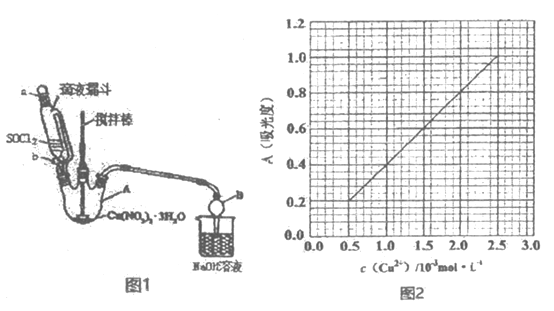
准确称取0.315 0g无水Cu(NO3)2,用蒸馏水溶解并定容至100mL,准确移取该溶液10.00mL,加过量NH3H2O,再用蒸馏水定容至100mL,测得溶液吸光度A=0.600,则无水Cu(NO3)2产品的纯度是_____(以质量分数表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.如图是H2O和CO反应生成CO2和H2过程中的能量变化示意图.由图可知,CO2和H2的总能量(填“大于”、“小于”或“等于”)H2O和CO的总能量,则该反应是(填“吸热”或“放热”)反应. 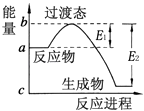
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、用0.1 molL-1 NaOH溶液分别滴定体积均为20.00 mL、浓度均为0.1 molL-1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
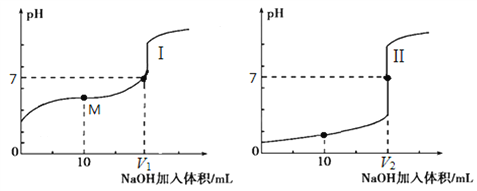
①滴定盐酸的曲线是______________(填“I”或“Ⅱ”);
②滴定开始前,三种溶液中由水电离出的c(H+)最大的是_____________________;
③V1和V2的关系:V1 _____ V2(填“>”、“=”或“<”)。
Ⅱ、已知25℃时,2.0×103 mol/L氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F)与溶液pH的变化关系如图所示。
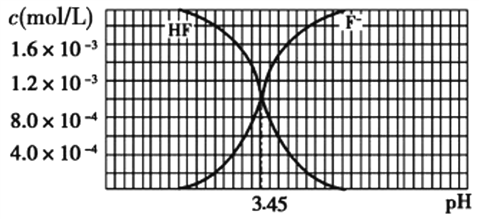
(1)25℃时,HF的电离平衡常数Ka=_____________。
(2)已知HF(aq)![]() H+(aq)+F(aq) ΔH=10.4 kJ/mol,现将室温下0.1 mol/L HF溶液升温至30℃(不考虑溶质和溶剂的挥发),下列各量增大的是__________。
H+(aq)+F(aq) ΔH=10.4 kJ/mol,现将室温下0.1 mol/L HF溶液升温至30℃(不考虑溶质和溶剂的挥发),下列各量增大的是__________。
a.Ka b.Kw c.n(H+) d. 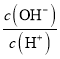
(3)25℃时,在20 mL 0.1 mol/L氢氟酸中加入V mL 0.1 mol/L NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是__________________。
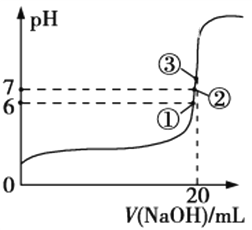
a.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
b.①点时pH=6,此时溶液中,c(F)c(Na+)=9.9×107 mol/L
c.②点时,溶液中的c(F)=c(Na+)
d.③点时V=20 mL,此时溶液中c(F)<c(Na+)=0.1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能在溶液中大量共存的一组离子是
A. NH4+、Ag+、PO43-、Cl-B. Fe3+、H+、I-、HCO3-
C. K+、Na+、NO3-、MnO4-D. Al3+、Mg2+、SO42-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列混合气体中,与同温同压同体积的CO气体原子数一定相等的是( )
A. HCl与O3 B. H2与NH3 C. N2与O2 D. He与NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法正确的是
A.淀粉、油脂和蛋白质都是高分子化合物
B.煤的气化和液化均属于化学变化
C.雾霾的发生与汽车尾气的直接排放无关
D.合成纤维和光导纤维都是新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与 Y同族,Z 与X 形成的离子化合物的水溶液呈中性。下列说法正确的是
A. 简单离子半径:W<X<Z
B. W与X形成的化合物溶于水后溶液呈碱性
C. 气态氢化物的热稳定性:W<Y
D. 最高价氧化物的水化物的酸性:Y>Z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com