
����Ŀ���������ں��졢DZ����ҽ�Ʒ���Ӧ�ù㷺����������[��Ҫ�ɷ�Ϊ��������(FeTiO3),������Fe2O3]Ϊԭ���Ʊ��ѵĹ���������ͼ��ʾ��
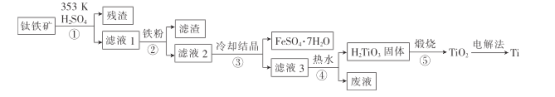
(1)����ڡ��ۡ�����,������еIJ�����_____________(���������)��
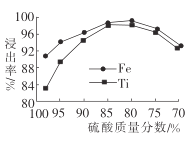
(2)��Һ1����Ԫ����TiO2+��ʽ����,�����������TiO2+�Ļ�ѧ����ʽΪ__________,���������������ѡ��������ʵ�Ӱ����ͼ��ʾ.�ݴ��ж�,���ʱ�����������������ӦΪ______(�Χ)��.
(3)�������ӷ���ʽ���Ͳ�����м���ˮ��ԭ��:__________��
(4)��ⷨ�Ʊ�Ti��װ������ʯīΪ����,TiO2Ϊ����,����CaOΪ����ʡ�Ti��_______(��������������������)���ɣ�____(������������������)������CaO����ʯ���顣
(5)���̷�Ϊԭ��,�����Ʊ���Ҫ��ҵԭ��������,������������:
![]()
���̷���Һ������Ũ���ɴ�С��˳��Ϊ__________��
��FeCO3�ﵽ�����ܽ�ƽ��ʱ,�����²����Һ��pHΪ8,c(Fe2+ )=1.0��10-5 mol��L-1������FeCO3��_____(������������������)��Fe(OH)2����֪: {Ksp[Fe(OH)2]= 4.9��10-17}
���𰸡����� FeTiO3+2H2SO4![]() FeSO4+TiOSO4+2H2O 80%~85% TiO2++ 2H2O
FeSO4+TiOSO4+2H2O 80%~85% TiO2++ 2H2O![]() H2TiO3+2H+��ˮ�ⷴӦ�����ȷ�Ӧ������ˮ�ٽ���Ӧ������Ӧ������� ���� ���� c(SO42-)>c(Fe2+)>c(H+)>c(OH-) ����
H2TiO3+2H+��ˮ�ⷴӦ�����ȷ�Ӧ������ˮ�ٽ���Ӧ������Ӧ������� ���� ���� c(SO42-)>c(Fe2+)>c(H+)>c(OH-) ����
��������
����������ܽ���˵õ�����TiO2+��Fe3+����Һ������Һ�м����ۻ�ԭFe3+�����˳�ȥ����������Һ��ȴ�ᾧ�����˵õ�FeSO47H2O�ͺ���TiO2+����Һ��������ˮ�ٽ�TiO2+ˮ������H2TiO3������H2TiO3����TiO2����������Ti���Դ˽����⡣
(1)���ݷ�����֪����ڡ��ۡ����У�������еIJ����ǹ��ˣ�
(2)��Ӧ��Ϊ�������Ԫ���غ��֪����ʽΪFeTiO3+2H2SO4![]() FeSO4+TiOSO4+2H2O������ͼ���֪��������������80%~85%֮��ʱ���������
FeSO4+TiOSO4+2H2O������ͼ���֪��������������80%~85%֮��ʱ���������
(3)TiO2+��ˮ��Һ�з���ˮ��TiO2++ 2H2O![]() H2TiO3+2H+��ˮ�ⷴӦ�����ȷ�Ӧ������ˮ�ٽ���Ӧ������Ӧ������У�����H2TiO3��
H2TiO3+2H+��ˮ�ⷴӦ�����ȷ�Ӧ������ˮ�ٽ���Ӧ������Ӧ������У�����H2TiO3��
(4)��TiO2����Ti��TiԪ�ػ��ϼ۽��ͷ�����ԭ��Ӧ�������������õ��ӷ�����ԭ��Ӧ��������ʯ���飬ʯ��������ˮ���������������������õ������ѣ����Բ��ܽ�����CaO����ʯ���飻
(5)���̷���Һ���������ӻᷢ��ˮ��ʹ��Һ�����ԣ�������Һ������Ũ���ɴ�СΪc(SO42-)>c(Fe2+)>c(H+)>c(OH-)��
�ڸ������⣬pHΪ8����c(OH-)=1��10-6mol/L����Ϊc(Fe2+)c2(OH-)=1.0��10-5��(1��10-6)2 =1.0��10-17��Ksp[Fe(OH)2]������Fe(OH)2���ɡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��LEDϵ�в�Ʒ�DZ����õ�һ������²�Ʒ,��ͼ��һ������ȼ�ϵ������LED�����װ�á������й�������ȷ����
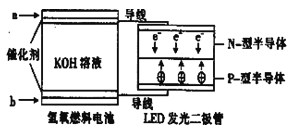
A��a��ͨ�������������˻�ԭ��Ӧ:H2-2e-+2OH-=2H2O
B��b��ͨ��������Ϊ��ص�����
C����װ����ֻ�漰������ʽ������ת��������е�KOH��ҺҲ����ϡ������Һ����
D��P-�Ͱ뵼�����ӵ��ǵ�ظ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��50 mL 0.50 mol��L1������50 mL 0.55 mol��L1 NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺
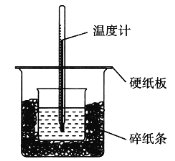
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ�����Ʒ��______________________________��
��2���ձ���������ֽ����������______________��
��3�����ձ����粻��Ӳֽ�壬��õ��к�����ֵ__________(����ƫ������ƫС��������Ӱ����)��
��4��ʵ���и���60 mL 0.50 mol��L1�����50 mL 0.55 mol��L1 NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų�������__________(��������������������)�������к���__________(��������������������)���������ɣ�_________________________��
��5������ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ��__________(����ƫ������ƫС��������Ӱ��������ͬ)����50 mL 0.50 mol��L1 NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����a��b��c��d�ĸ������缫��GΪ�����ơ��йصķ�Ӧװ�ü����ַ�Ӧ�������£�
ʵ��װ�� |
|
|
|
|
����ʵ������ | a��������С��b���������� | ��Һ�е�SO42-��b���ƶ� | d���ܽ�c����������� | ���Ӵ�d������a�� |
�ɴ˿��ж������ֽ����Ļ��˳����
A. d>a>b>cB. a>b>c>dC. b>c>d>aD. a>b>d>c
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������MnO2��Ũ�����������ķ�ӦΪMnO2��4HCl(Ũ)![]() MnCl2��2H2O��Cl2������Ӧ�У������17.4 g MnO2����ԭ����ô��
MnCl2��2H2O��Cl2������Ӧ�У������17.4 g MnO2����ԭ����ô��
(1)������Cl2�ڱ�״���µ����Ϊ__________;
(2)ת�Ƶ��ӵ����ʵ���Ϊ_______________;
(3)��֯��ҵ�г���������Ư����Ư�ײ�ƥ����������Ҫ��ȥ��ͨ������Na2SO3�������ȼ��������Ⱥ�IJ���ΪNa2SO4���ȱ�Ϊ��1�ۡ����ѱ����в�����Cl2��ȫת������ҪNa2SO3������Ϊ____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ�о���ѧϰС���ijNa2CO3��NaHCO3�Ļ����Һ����ɽ���̽����ȡ20.0mL�û����Һ�������в��ϼ���1.00mol��L��1��ϡ���ᣬ����ϡ���������Ͳ����������������ʾ��
��Ӧ�� | �� | �� | �� |
ϡ�������x/mL | 0��x��10.0 | 10.0��x��40.0 | x��40.0 |
�֡����� | ������ | ������ | ������ |
������Һ��c��HCO3����Ϊ��������
A. 1.00mol��L��1 B. 0.50mol��L��1 C. 1.50mol��L��1 D. 2.00mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������ֻ��A��B��C���ֵ��ʣ�A����ɫ��ӦΪ��ɫ����Ҫ��G��ʽ�����ں�ˮ�У�F��һ�ֵ���ɫ�Ĺ��壬H��һ�ֳ�������ɫҺ�壬I���������ЧӦ����Ԫ�����������ʼ��ת����ϵͼ���£�
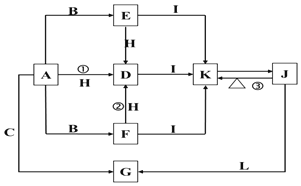
�밴Ҫ����д��
��1����Ӧ�ٵ����ӷ���ʽ�� ____________________________________��
��2������K������L�����ʵ������ӷ���ʽ��___________________________��
��3������Fת��ΪD�����ӷ���ʽ��___________________________________��
��4������G������Jת���Ļ�ѧ����ʽ��_______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���a L�ܱ������м���1 mol X�����2 mol Y���壬�������·�Ӧ��X(g)+2Y(g)![]() 3Z(g)���˷�Ӧ�ﵽƽ��ı�־��
3Z(g)���˷�Ӧ�ﵽƽ��ı�־��
A. ������ѹǿ����ʱ��仯
B. �����ڸ����ʵ�Ũ�Ȳ���ʱ��仯
C. ������X��Y��Z��Ũ��֮��Ϊl��2��3
D. ��λʱ������0.1 mol Xͬʱ����0.3 mol Z
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ü�������������ȡ����Ӧ��ȡ����Ʒ����������ڹ�ҵ���ѳ�Ϊ��ʵ��ij��ѧ��ȤС��ͨ����ʵ������ģ���������̣�����Ƶ�ģ��װ�����£�

�������Ҫ��ش�
��1��Bװ�������ֹ��ܣ������������ٶȣ� �����Ȼ�����壻 ��____________��
��2����![]() ��x��������������������Ȼ��⣬��xȡֵ��Χ________��
��x��������������������Ȼ��⣬��xȡֵ��Χ________��
��3��Dװ�õ�ʯ���о��Ȼ���KI��ĩ����������______________��
��4��Eװ�õ�������________�����ţ���
A �ռ����� B ��������
C ��ֹ���� D �����Ȼ���
��5����Cװ���У�����һ��ʱ���ǿ�����䣬����Ӳ�ʲ������ڱ��к�ɫС����������д���û�����ɫС�����Ļ�ѧ����ʽ��_______________________________________��
��6��Eװ���г����������⣬�������л����E�з�����л������ѷ���Ϊ________����װ�û���ȱ�ݣ�ԭ����û�н���β����������β����Ҫ�ɷ�Ϊ________�����ţ���
a CH4 b CH3Cl c CH2Cl2 d CHCl3 e CCl4
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com