
嫦娥二号月球探测器获得了7 m分辨率全月球影像图,该月球探测器使用钚元素的同位素电池来提供稳定、持久的能源。下列关于 Pu的说法正确的是( )
Pu的说法正确的是( )
A. Pu和
Pu和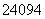 Pu的质子数之差为2
Pu的质子数之差为2
B. Pu和
Pu和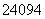 Pu是两种不同的核素
Pu是两种不同的核素
C. Pu的中子数与质子数之差为144
Pu的中子数与质子数之差为144
D. Pu和
Pu和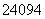 Pu互为同素
Pu互为同素 异形体
异形体
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
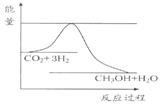 (1)关于该反应的下列说法中,其△H 0。(填“大于”、“小于”或“等于”), 且在 (填“较高”或“较低”)温度下有利于该反应自发进行。
(1)关于该反应的下列说法中,其△H 0。(填“大于”、“小于”或“等于”), 且在 (填“较高”或“较低”)温度下有利于该反应自发进行。
(2)该反应平衡常数K的表达式为 。
(3)温度降低,平衡常数K (填“增大”、“不变”或“减小”)。
(4)若为两个容积相同的密闭容器,现向甲容器中充入1 mol CO2(g)和3 molH2(g),乙容器中充入1mol CH3OH(g)和1 mol H2O(g),在相同的温度下进行反应,达到平衡时,甲容器内n(CH3OH) (填“大于”“小于”或“等于”)乙容器内n(CH3OH)。
(5)已知:CO(g)+2H2(g) = CH3OH (g) △H= -116 kJ•mol-1;CO(g)+1/2O2(g)=CO2(g)
△H=-283 kJ•mol-1 ;H2 (g)+1/2O2(g)=H2O(g) △H=-242 kJ•mol-1 ,写出CH3OH燃烧生成CO2和水蒸气的热化学方程式______________________________________。
(6)以甲醇和氧气为燃料,氢氧化钾溶液为电解质溶液构成电池。
①负极的电极反应式为 。
②若以石墨为电极,电解硫酸铜溶液,写出电解的总反应方程式 。若以此燃料电池电解200 mL 0.8mol/L的硫酸铜溶液,当消耗1.6甲醇时,在阴极会析出 g铜。
查看答案和解析>>
科目:高中化学 来源: 题型:
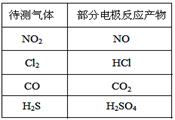
气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散 进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是( )

A.上述气体检测时,敏感电极均作电池正极
B.检测Cl2和NO2体积分数相同的两份空气样本时,传感器上产生的电流大小相同
C.检测H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小相同
D.检测H2S时,对电极充入空气,对电极上的电极反应式为O2 + + 4e-===2O2-
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D、E、F、G和X八种物质存在如下图所示的转化关系。其中C是过渡元素的单质,其他元素均是短周期元素;B的浓溶液和稀溶液都能与C反应,但还原产物不同;反应⑤用于传统制镜工业,X是医疗上病人重要的营养补给物质(通过输液);F是大气污染物,也是汽车尾气的成分之一。请回答下列问题:(部分生成物未标出)
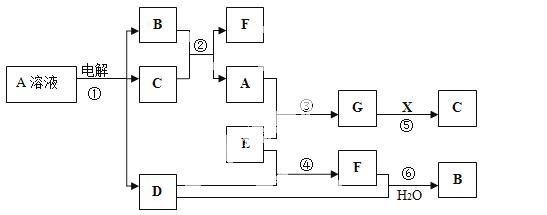
(1)A、X的化学式分别是 , ;G溶液俗称为 。
(2)写出反应①的离子方程式 。
(3)写 出E的分子式 ,请用电离方程式解释E的水溶液呈碱性的原因
出E的分子式 ,请用电离方程式解释E的水溶液呈碱性的原因
。
(4)已知1gE与足量的空气混合,在加热及有催化剂存在下发生反应生成气态产物,放出热量13.3kJ,请写出该反应的热化学方程式 。
(5)为了消除F对大气的污染,工业上采用在催化剂作用下E与F反应,将其转化为无毒气体和水,请写出该反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是一些重要工业生产的转化关系(反应条件略去)。
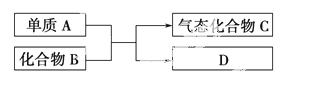
请完成下列问题:
(1)若D是单质,且与A属于同一主族,则:
①反应的化学方程式是_____________________________________________
_______________________________。
②D的原子结构示意图是________。
③D单质的一种重要用途是_________________________ _______________________________。
_______________________________。
(2)若B为黄色固体,D为固体化合物,则:
①该反应的化学方程式是 ___________________________________________________。
___________________________________________________。
②生产该工业品的工厂应建在离________较近的地方。
③实验室检验C的方法是______________________________________________________。
(3)若B是一种有刺激性气味的气体,则:
①B分子的空间构型为________。
②实验室进行此实验时,常看到有大量白烟 产生,产生大量白烟的原因是___________________________________________
产生,产生大量白烟的原因是___________________________________________ _________________。
_________________。
③化合物C在一定体积的容器中,在一定条件下发生反应,测得容器内气体的压强略小于原来的 。请写出该反应的化学方程式________________________________________________________。
。请写出该反应的化学方程式________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素的原子最外层只有一个电子,它跟卤素结合时,所形成的化学键( )
A.一定是离子键
B.一定是共价键
C.可能是离子键,也可能是共价键
D.以上说法都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是________。
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为________,氧化性最弱的简单阳离子是________。
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 1 |
工业制镁时,电解MgCl2而不电解MgO的原因是__________________________________;
制铝时,电解Al2O3而不电解AlCl3的原因是______________________________。
(4)晶体硅(熔点1410 ℃)是良好的半导体材料。由粗硅制纯硅过程如下:
Si(粗)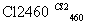 SiCl4
SiCl4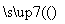 SiCl4(纯)
SiCl4(纯)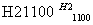 Si(纯)
Si(纯)
写出SiCl4的电子式:________________;在上述由SiCl4制纯硅的反应中,测得每生成1.12 kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:______________________________________________
______ __________________________________________________________________。
__________________________________________________________________。
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是________。
a.NH3 b.HI c.SO2 d.CO2
c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400 ℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:
___________________________________________________________________ _____。
_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z均为短周期元素。已知X元素的某种原子核内无中子,Y元素的原子核外最外层电子数是其次外层电子数的2倍,Z元素是地壳中含量最丰富的元素。有下列含这三种元素的化学式:
①X2Y2Z2 ②X2YZ3 ③X2YZ2 ④X2Y2Z4
⑤X3YZ4 ⑥XYZ3,其中可能存在的是( )
A.② B.②④⑤
C.②⑤⑥  D.①②③④
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
有一块质量为n g的铁片浸入V mLCuSO4溶液中,待CuSO4溶液中的铜全部析出后,把附有铜的铁片取出干燥,再称重为m g,设反应前后溶液的体积不变,则原CuSO4溶液的物质的浓度为( )
A.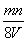 mol·L-1
mol·L-1
B.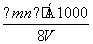 mol·L-1
mol·L-1
C.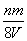 mol·L-1
mol·L-1
D.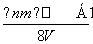 mol·L-1
mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com