
���� ��1��0.1mol•L-1��NaOH��Һ��c��OH-��=0.1mol/L������Kw=c��H+��•c��OH-��������Һ��c��H+�����ٸ���pH=-lgc��H+��������Һ��pHֵ��
��2����Һ�д��ڵ���ƽ�⣬Ӧ����������ʣ�
��3����������ˮ���룬�����������ӵ��δٽ�ˮ���룻
��4��������Ϊ������ʣ��ζ��յ�ʱ����Һ�ʼ��ԣ�
��NaOH������ǡ�÷�Ӧʱ������20mlNaOH��Һ����������ǿ���Σ���Һ�ʼ��ԣ�
��� �⣺��1��0.1mol•L-1��NaOH��Һ��c��OH-��=0.1mol/L������Һ��c��H+��=$\frac{1��1{0}^{-14}}{0.1}$mol/L=10-13mol/L���ʸ���Һ��pH=-lg10-13=13���ʴ�Ϊ��13��
��2��0.1mol•L-1��CH3COOH��Һ�д����ܼ�ˮ��ˮΪ������ʣ���������Ϊ������ʣ����ڵ���ƽ��ΪCH3COOH?CH3COO-+H+��H2O?OH-+H+��
�ʴ�Ϊ��CH3COOH?CH3COO-+H+��H2O?OH-+H+��
��3����������ˮ���룬�����������ӵ��δٽ�ˮ���룬������������ʣ��������ơ��Ȼ�����ǿ����ʣ�������ͬ���ʵ���Ũ�ȵ������������������ƣ�������ˮ�����������������Ũ��С�ڴ��ᣬ��ͬ���ʵ���Ũ�ȵ�������������ƶ�ˮ�������Ƴ̶���ȣ�������ˮ�����������������Ũ�ȵ�������������Һ��ˮ�ĵ��룬����ˮ���������������Ũ�ȴ�С˳���ǣ�������=�ң�
�ʴ�Ϊ��������=�ң�
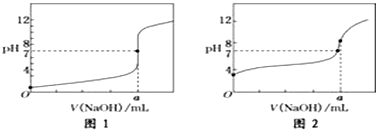
��4���ٴ���Ϊ������ʣ��ζ�������pH�仯�����Ỻ�����ζ��յ�ʱ��Һ�ʼ��ԣ���ζ�������Һ��������ͼ2���ʴ�Ϊ��ͼ2��
�ڵζ��յ�ʱn��CH3COOH��=n��NaOH������a=20.00mL����Ӧ�����˴����ƣ���������ӷ���ˮ�⣬CH3COO-+H2O?CH3COOH+OH-����Һ��ʾ����pH��7��
�ʴ�Ϊ��20.00��
���� �����ۺϿ�������ϵĶ����жϼ���ҺpH�ļ��㣬��Ŀ�Ѷ��еȣ���ȷ��Һ���������ҺpH�Ĺ�ϵ���ͼ������ж��ǽ����ؼ�������������ѧ���ķ������������������Ӧ����ѧ֪ʶ��������


 ����ѧ��Ӧ�����ϵ�д�
����ѧ��Ӧ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
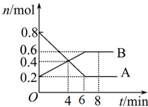 ij�¶�ʱ����2L�ܱ�������ijһ��Ӧ��A��B���ʵ�����ʱ��仯��������ͼ��ʾ��
ij�¶�ʱ����2L�ܱ�������ijһ��Ӧ��A��B���ʵ�����ʱ��仯��������ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �������� | �������� | ʵ��Ԥ�� | |
| A | Ũ��ˮ | ��̪��Һ | ������Һ��Ϊ��ɫ |
| B | Ũ���� | ����KI��Һ | ������Һ��Ϊ��ɫ |
| C | Ũ���� | Ũ��ˮ | ���ձ����а��� |
| D | ���͵���������Һ | ϡ��ˮ | ���������Ա仯 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
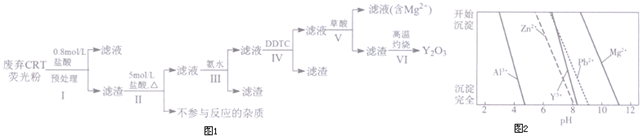
| �ɷ� ����/% �� | Y2O3 | ZnO | Al2O3 | PbO2 | MgO |
| Ԥ����ǰ | 24.28 | 41.82 | 7.81 | 1.67 | 0.19 |
| Ԥ������ | 68.51 | 5.42 | 4.33 | 5.43 | 0.50 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| װ�� |  |  |  |
| ���� | ���۽���A�����ܽ� | C���������� | A����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
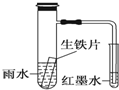
| A�� | ����Ƭ�е�̼��ԭ��صĸ�����������ԭ��Ӧ | |
| B�� | ��ˮ���Խ�ǿ������Ƭʼ�շ������ⸯʴ | |
| C�� | ��֧�Թ�����Һ������ǿ | |
| D�� | īˮ����ʱ��̼�缫��ӦʽΪO2+2H2O+4e-�T4OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{c��O{H}^{-}��•c��N{H}_{4}^{+}��}{c��N{H}_{3}•{H}_{2}O��}$ | B�� | $\frac{c��N{H}_{3}•{H}_{2}O��}{c��O{H}^{-}��}$ | ||
| C�� | c��H+����c��OH-���ij˻� | D�� | OH-�����ʵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3d | B�� | 5f | C�� | 6p | D�� | 7s |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com