
| A、a>b | B、a<b |
| C、a=b | D、不能确定 |
| 5 |
| 24 |
| 5 |
| 24 |


 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
| A、铁锈的形成一定发生了氧化还原反应 |
| B、复分解反应都不是氧化还原反应 |
| C、燃烧都是放热反应,也都是氧化还原反应 |
| D、分解反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝元素在地壳中的含量高,储量丰富 |
| B、铝容易形成致密的氧化膜,抗腐蚀性能好 |
| C、铝的冶炼技术基本成熟,可以大量生产铝 |
| D、化学性质稳定,常温下不与任何酸碱反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4与C4H10互为同系物 |
| B、C5H12有三种同分异构体 |
| C、甲烷与氯气在光照条件下能发生取代反应 |
| D、所有烷烃中均有碳碳单键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2中 |
| B、SO2和SO3中 |
| C、SO2和O2中 |
| D、SO2、SO3和O2中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
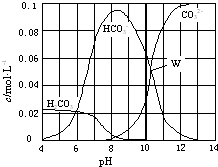 25℃时,0.1mol Na2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH 的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )
25℃时,0.1mol Na2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH 的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )| A、W点所示的溶液中:c(CO32-)=c(HCO3-)>c(OH-)>c(H+) |
| B、pH=4的溶液中:c(H2CO3)+c(HCO3-)+c(CO32-)=0.1mol?L-1 |
| C、pH=8的溶液中:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) |
| D、pH=11的溶液中:c(Na+)+c (H+)=c(OH-)+c(Cl-)+c(CO32-)+c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c?H2? |
| c?CH3OH? |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com