
| A. | 稳定性:NH3<PH3<AsH3 | B. | 离子半径:阴离子>阳离子 | ||
| C. | 熔沸点:离子化合物>共价化合物 | D. | 酸性:H2SO4>H3PO4>H2SiO3 |
分析 A.元素非金属性越强,其氢化物的稳定性越强;
B.离子半径与离子电子层数成正比,电子层结构相同的离子,离子半径随着原子序数增大而减小;
C.一般离子化合物的熔点较高,但不一定大于共价化合物的熔沸点;
D.元素非金属性越强,其最高价氧化物的水化物酸性越强.
解答 解:A.元素非金属性越强,其氢化物的稳定性越强,非金属性N>P>As,则氢化物的稳定性NH3>PH3>AsH3,故A错误;
B.离子半径与离子电子层数成正比,电子层结构相同的离子,离子半径随着原子序数增大而减小,所以阴离子半径不一定大于阳离子半径,如F-<K+,故B错误;
C.二氧化硅为共价化合物,氯化钠为离子化合物,但二氧化硅的熔沸点大于氯化钠的,故C错误;
D.元素非金属性越强,其最高价氧化物的水化物酸性越强,非金属性S>P>Si,所以H2SO4>H3PO4>H2SiO3,故D正确;
故选D.
点评 本题考查非金属性的比较、熔沸点的比较、微粒半径的比较,为高频考点,侧重考查学生分析判断能力,明确物质构成、元素周期律是解本题关键,注意规律中的反常现象,易错选项是C.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | Li和Na | B. | Rb和Ca | C. | Na和Cu | D. | K和Na |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
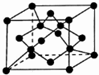 原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种:1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种:1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
| 熔点/K | 993 | 1539 | 183 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂解、煤的气化、海水制镁等过程中都包含化学变化 | |
| B. | 在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源 | |
| C. | 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强酸、强碱都会“断路” | |
| D. | 硬脂酸甘油酯在碱性条件下的水解属于皂化反应,乙酸乙酯在碱性条件下的水解不属于皂化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
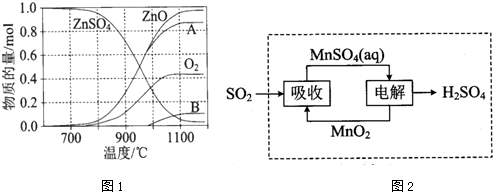
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 甲烷的球棍模型: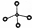 | |
| B. | 乙炔的结构简式:CH=CH | |
| C. | 3-甲基-1-丁烯的结构简式:(CH3)2CHCH=CH2 | |
| D. | 羟基的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 橙花醛不可以与溴发生加成反应 | |
| B. | 1mol橙花醛最多可以与2mol氢气发生加成反应 | |
| C. | 橙花醛可以发生银镜反应,分子结构存在顺反异构 | |
| D. | 橙花醛是乙醛的同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ⑦CH3CH2OH中与甲烷互为同系物的是①,分子空间构型为平面形的是④⑥,直线形的是⑤.
⑦CH3CH2OH中与甲烷互为同系物的是①,分子空间构型为平面形的是④⑥,直线形的是⑤.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com