
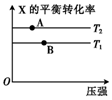
 向某密闭容器中充入1mol X与2mol Y发生反应:X(g)+2Y(g)?aZ(g)△H<0,达到平衡后,改变某一条件(温度或容器体积),X的平衡转化率的变化如图所示.下列说法中正确的是( )
向某密闭容器中充入1mol X与2mol Y发生反应:X(g)+2Y(g)?aZ(g)△H<0,达到平衡后,改变某一条件(温度或容器体积),X的平衡转化率的变化如图所示.下列说法中正确的是( )| A. | a=2 | B. | T2>T1 | ||
| C. | A点的反应速率:3v正(X)=v逆(Z) | D. | 表示A、B两点的反应速率:v(A)>v(B) |
分析 A.由图可知,压强不影响平衡移动,则反应为气体体积不变的反应;
B.该反应为放热反应,升高温度平衡逆向移动,转化率减小;
C.A点为平衡点,不同物质的正逆反应速率之比等于化学计量数之比;
D.温度越高,反应速率越快.
解答 解:A.由图可知,压强不影响平衡移动,则反应为气体体积不变的反应,则a=1+2=3,故A错误;
B.该反应为放热反应,升高温度平衡逆向移动,转化率减小,则T2<T1,故B错误;
C.A点为平衡点,不同物质的正逆反应速率之比等于化学计量数之比,则A点的反应速率:3v正(X)=v逆(Z),故C正确;
D.温度越高,反应速率越快,T2<T1,则v(A)<v(B),故D错误;
故选C.
点评 本题考查化学平衡的影响因素,为高频考点,把握温度、压强对化学平衡的影响为解答的关键,侧重分析与应用能力的考查,注意图象与平衡移动原理的结合,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验自来水中是否含有氯离子 | B. | 检验土豆中是否含有淀粉 | ||
| C. | 检验鸡蛋中是否含有碳酸钙 | D. | 检验无水酒精中是否含水 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 溶液X中一定含有Na+、Cl-和SiO32- | |
| B. | 溶液X中一定不含Ca2+、Br- | |
| C. | 为确定溶液X中是否含有SO42-,可取溶液2,加入BaCl2溶液 | |
| D. | 在溶液X中依次滴入盐酸、双氧水和硫氰化钾溶液后,溶液将变为红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定不含 I- | B. | 肯定不含 SO42- | C. | 可能含有 SO32- | D. | 肯定含有 NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有化学键断裂或化学键形成的过程都是化学变化 | |
| B. | Na2O2和Na2O都属于碱性氧化物 | |
| C. | 溶液中的溶质粒子能透过滤纸,而胶体中的分散质粒子不能透过滤纸,所以可以用滤纸来分离溶液和胶体 | |
| D. | 食盐溶液能导电,但食盐溶液不是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 古文 | 解释 |
| A | 烧酒非古法也,自元时创始,其法用浓酒和糟入甑(指蒸锅),蒸令气上,用器承滴露 | 白酒(烧酒)的制造过程中采用了蒸馏的方法来分离和提纯 |
| B | 白青(碱式碳酸铜)得铁化为铜 | 可以用铁来冶炼铜 |
| C | 初,人不知盖泥法,元时南安有黄长者为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之 | 蔗糖的分离提纯采用了黄泥来吸附红糖中的色素 |
| D | 丹砂烧之成水银,积变又成丹砂 | 加热时丹砂(HgS)熔融成液态,冷却时重新结晶为HgS晶体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com