
某研究性小组用含铬废水制取具有强氧化性的重铬酸钾(K2Cr2O7),实验方案如下:

已知:
①Cr2O72-(橙色)+H2O 2CrO42-(黄色)+2H+
2CrO42-(黄色)+2H+
②金属离子沉淀的PH如下:
离子 | 开始沉淀的PH | 沉淀完全的PH |
Cr3+ | 4.9 | 6.8 |
Fe3+ | 1.5 | 4.1 |
③不同温度下化合物的溶解度如下:
物质 | 溶解度/(g/110g水) | ||
0℃ | 40℃ | 80℃ | |
K2SO4 | 7.4 | 14.8 | 21.4 |
K2Cr2O7 | 4.7 | 26.3 | 73 |
请回答:
(1)操作A的名称是____,加入硫酸的目的是_____。
(2)写出固体1中加入H2O2和KOH溶液后发生反应的离子方程式________。
(3)操作B由多步组成,获得K2Cr2O7晶体的操作依次是:蒸发浓缩、操作1、洗涤1、操作2、抽滤、洗涤2、干燥。则下列说法正确的是__________。
A.操作1和操作2分别是趁热过滤和冷却结晶
B.洗涤1和洗涤2所用的洗涤剂分别为0℃的冷水和80℃的热水
C.当溶液出现过饱和现象时,振荡容器或用玻璃棒轻轻摩擦器壁均可促使晶体析出
D.进行洗涤2操作时,可用摩尔盐[(NH4)2SO4·FeSO4·6H2O]标准溶液滴定,反应的离子方程式:
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
①请简述将已用移液管吸取的待测液转移至锥形瓶中的操作__________。
②滴定时,先称取0.5000g K2Cr2O7 产品,溶于水配成100mL溶液,用0.1000mol/L的摩尔盐标准溶液进行滴定,数据记录如下:
实验序号 | 待测样品溶液的体积/mL | 0.1000mol/L摩尔盐溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.00 | 24.98 |
2 | 25.00 | 1.56 | 29.30 |
3 | 25.00 | 1.00 | 26.02 |
则测得K2Cr2O7产品的纯度是_________(以质量分数表示)。
科目:高中化学 来源:2016-2017学年河北省张家口市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 用直接加热并蒸干FeCl3溶液的方法可制得纯净的无水FeCl3
B. 等物质的量浓度的Na2CO3溶液和CH3COONa溶液的pH,前者大于后者
C. 中和等体积、等物质的量浓度的盐酸和醋酸溶液,消耗NaOH的物质的量不相等
D. 对于有气体参加的反应,增大气体反应物浓度,活化分子百分数增大,反应速率加快
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省大连市高二上学期期末考试(文)化学试卷(解析版) 题型:简答题
根据所学知识回答:
(1)近年来,我国高铁迅猛发展,为人们的出行带来便利。人们利用如下反应焊接铁轨:8Al+3Fe3O4  4Al2O3+9Fe。该反应是______(填“放热”或“吸热”)反应,反应中的还原剂是________(填化学式)。
4Al2O3+9Fe。该反应是______(填“放热”或“吸热”)反应,反应中的还原剂是________(填化学式)。
(2)钠元素有NaCl、Na2O2、NaHCO3、Na2SiO3等多种重要的化合物。请根据题意选择钠的化合物的化学式填空:其中常用来作为潜水艇和呼吸面具中氧气来源的淡黄色固体是________,常用来烘制糕点,也可用作抗酸药的是_________。
(3)向FeCl2溶液中通入Cl2,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-。向所得溶液中滴加KSCN溶液,溶液变成________色,我们可以利用这一现象检验Fe3+的存在。
查看答案和解析>>
科目:高中化学 来源:2017届山西省名校高三下学期联考理综化学试卷(解析版) 题型:简答题
2014年7月和12月山西大学分子科学研究所翟华金教授、李思殿教授与清华大学李隽教授、美国布朗大学Lai-Sheng Wang教授及复旦大学刘智攀教授课题组合作,首次合成“中国红灯笼分子”——硼球烯B40。B40是继C60之后第二个从实验和理论上完全确认的无机非金属笼状团簇。
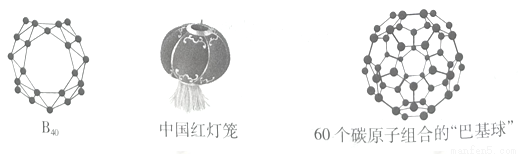
(1) 基态硼原子的外围电子排布式为___________,碳60中碳原子杂化方式为____________。
(2)构成碳60晶体的作用力是___________________。
⑶与硼同周期但第一电离能比硼大的元素有___________种。
(4)磷化硼(BP)是由硼元素与磷元素组成的无机化合物,属于一种半导体材料。磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成。BP晶胞中B采用面心立方堆积,P原子填入四面体空隙中。
①写出三溴化硼和三溴化磷的空间构型:
三溴化硼__________;三溴化磷____________。
②磷化硼晶体内微粒间的作用力有__________。
③计算磷化硼中硼原子和磷原子之间的最近距离(晶胞参数为478pm)____________ 。
查看答案和解析>>
科目:高中化学 来源:2017届山西省名校高三下学期联考理综化学试卷(解析版) 题型:选择题
NA为阿伏伽德罗常数的值。下列说法正确的是
A. 10.6g碳酸钠溶于水,其中CO32-和HCO3-的微粒数之和为0.1NA
B. 甲醇燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为6NA
C. 常温常压下,22.4 L SO2中含有的分子数小于6.02×1023
D. 6.4 g CaC2中所含的共价键数为0.2NA
查看答案和解析>>
科目:高中化学 来源:浙江省台州市2017届高三2月选考科目教学质量评估测试化学试卷 题型:简答题
乙酸乙酯是非常重要的有机溶剂和化工原料,下图转化关系中的①、②、③是工业上合成乙酸乙酯的常见反应,其中A是一种常见的调味品。请回答:
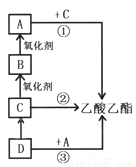
(1)有机物A中含有的官能团名称是____________。
(2)写出反应①的化学方程式_____________。
(3)已知反应②在催化剂作用下无需加入其他反应物即可一步合成产物,同时生成一种无色无味气体,该气体的化学式为_________。
(4)下列说法正确的是_________
A.将D通入溴水中,溴水褪为无色,原因是D与Br2发生了取代反应
B.C B、B
B、B A的氧化剂可以相同,也可以不同
A的氧化剂可以相同,也可以不同
C.反应③是①、②、③中唯一符合绿色化学的“零排放”要求的
D.已知量分子B可以通过一步反应生成乙酸乙酯,则同时有水生成
查看答案和解析>>
科目:高中化学 来源:浙江省台州市2017届高三2月选考科目教学质量评估测试化学试卷 题型:选择题
根据能量变化示意图,下列说法正确的是
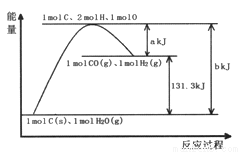
A. 1molC和1molH2O反应生成1molCO和1molH2一定吸收131.3kJ的热量
B. 反应的热化学方程式可表示为C(s)+H2O(g)=CO(g)+H2(g) ΔH=(a-b)KJ/mol
C. 该反应过程反应物断键吸收的能量要小于生成物成键放出的能量
D. 加入适当的催化剂,可以加快正、逆反应速率
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二下学期基础训练(15)化学试卷(解析版) 题型:选择题
已知一个N2O3分子的质量为a g,一个N2O5分子的质量为b g,若以一个氧原子质量的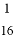 作为相对原子质量的标准,则NO2的相对分子质量为
作为相对原子质量的标准,则NO2的相对分子质量为
A. 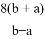 B.
B. 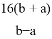 C.
C.  D.
D. 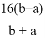
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com