
| A. | Al2O3用作耐火材料、Al(OH)3用作阻燃剂 | |
| B. | 碳素钢的主要成分是铁碳合金、司母戊鼎的主要成分是铜锡合金 | |
| C. | 自然界中不存在游离态的硅,硅主要以二氧化硅和硅酸盐的形式存在 | |
| D. | 通过化学变化可以实现12C与14C间的相互转化 |
分析 A.Al2O3熔点高、Al(OH)3加热易分解;
B.碳素钢是一种铁的合金,司母戊鼎的主要成分是铜锡合金;
C.硅是亲氧元素在自然界中不存在游离态的硅;
D.12C与14C之间的转化是原子核的变化.
解答 解:A.Al2O3熔点高、Al(OH)3加热易分解,可用于阻燃剂,故A正确;
B.碳素钢是一种铁的合金,司母戊鼎的主要成分是铜锡合金,故B正确;
C.硅为亲氧元素,在自然界中主要以二氧化硅和硅酸盐的形式存在,故C正确;
D.12C与14C之间的转化,属于核变化,不是化学变化,故D错误;
故选D.
点评 本题综合考查元素及其化合物的性质,为高考高频考点,侧重于元素化合物知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案科目:高中化学 来源: 题型:选择题
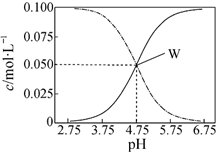
| A. | pH=5.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | W点表示溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| C. | 向W点所表示的1.0L溶液中通入0.05molHCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH-) | |
| D. | pH=3.5溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②④ | C. | ②③ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
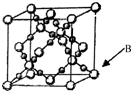 某原料经测定主要含有A、B、C、D、E五种前四周期元素,且原子序数依次增大.元素A、B、C、D、E的原子结构等信息如下:
某原料经测定主要含有A、B、C、D、E五种前四周期元素,且原子序数依次增大.元素A、B、C、D、E的原子结构等信息如下:| 元素 | 元素性质或原子结构 |
| A | 周期表中原子半径最小 |
| B | 原子核外有三种不同的能量的原子轨道且各个轨道所填充的电子数相同 |
| C | 最外层p轨道半充满 |
| D | 位于短周期,其原子的核外成对电子数是未成对电子数的3倍 |
| E | 位于ds区且原子的最外层电子数与A的相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向反应后的溶液中继续加入少量铁粉,铁粉可以继续溶解 | |
| B. | 氧化性:Ag+>Fe3+>Cu2+>Zn2+ | |
| C. | 反应后溶液的质量减轻 | |
| D. | 反应后溶液中Cu2+与Fe2+的物质的量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三月考二化学试卷(解析版) 题型:推断题
有机化学反应因反应条件不同,可生成不同的有机产品。例如:
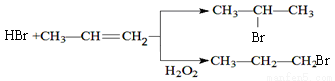
工业上利用上述信息,按下列路线合成结构简式为 的物质,该物质是一种香料。
的物质,该物质是一种香料。
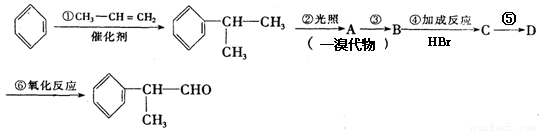
请根据上述路线,回答下列问题:
(1)A的结构简式可能为 。
(2)反应③、⑤的反应类型分别为 、 。
(3)反应④的化学方程式为(注明反应条件): 。
(4)工业生产中,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法,其原因是___________。
(5)这种香料是具有多种同分异构体,其中某种物质有下列性质:
①该物质的水溶液遇FeCl3溶液呈紫色
②分子中有苯环,且苯环上的一溴代物有两种。
写出符合上述两条件的物质可能的结构简式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com