
| A. | 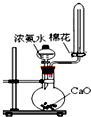 制氨气 | B. | 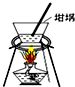 蒸发、浓缩、结晶 | ||
| C. | 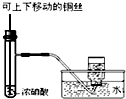 制备并收集少了二氧化氮 | D. | 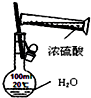 浓硫酸稀释 |
分析 A.CaO和水反应是放热反应,一水合氨分解是吸热反应,所以可以用浓氨水和CaO混合制取氨气,根据氨气密度和性质选取合适的收集方法;
B.用于蒸发浓缩、冷却结晶的仪器是蒸发皿;
C.二氧化氮气体能溶于水,不能采用排水法收集;
D.容量瓶只能配制一定物质的量浓度溶液,但不能稀释或溶解药品.
解答 解:A.CaO和水反应是放热反应,一水合氨分解是吸热反应,所以可以用浓氨水和CaO混合制取氨气,氨气密度小于空气且常温下和空气不反应,所以可以采用向下排空气法收集,故A正确;
B.用于蒸发浓缩、冷却结晶的仪器是蒸发皿,坩埚用于高温灼烧固体药品,故B错误;
C.二氧化氮气体能溶于水,不能采用排水法收集,应该采用向上排空气法收集,故C错误;
D.容量瓶只能配制一定物质的量浓度溶液,但不能稀释或溶解药品,应该用烧杯稀释浓硫酸,将溶液冷却至室温后再转移到容量瓶中,故D错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及气体制取和收集、溶液配制、仪器的选取等知识点,明确实验原理、实验基本操作方法、仪器的用途等是解本题关键,注意容量瓶的用途及规格,题目难度不大.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:解答题
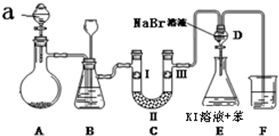
| a | b | c | d | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 无水氯化钙 | 浓硫酸 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

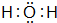 D 的原子结构示意图
D 的原子结构示意图 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 达到化学平衡后,增加A的量有利于化学平衡向正反应方向移动 | |
| B. | 达到平衡后,若使温度升高,化学平衡向逆反应方向移动 | |
| C. | 化学方程式中n<c+f | |
| D. | 达到平衡后,若使用催化剂,C的体积分数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol乙炔分子所含的共用电子对总数为5NA | |
| B. | 1 mol甲基(-CH3 )所含的电子总数为9NA | |
| C. | 0.5 mol 1,3-丁二烯分子中含有碳碳双键总数为NA | |
| D. | 标准状况下,22.4L己烷完全燃烧所生成的气态产物的分子数为7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③④⑤ | C. | ①②③④⑥ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 步骤 | 操作 | 现象 |
| (1) | 用紫色石蕊试液检验 | 溶液变红 |
| (2) | 向溶液中滴加BaCl2和稀HCl | 有白色沉淀生成 |
| (3) | 将(2)中所得混合物过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀生成 |
| A. | 肯定含有的离子是②③⑥ | B. | 肯定没有的离子是④⑤ | ||
| C. | 可能含有的离子是①③ | D. | 可能含有的离子是① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com