
【题目】在25°C时,向amL0.10mol·L-1的HNO2溶液中逐滴加入0.10mol·L-1的NaOH溶液。滴定过程中混合溶液的pOH[pOH=-lgc(OH-)]与NaOH溶液的体积V的关系如图所示。已知P点溶液中存在c(OH-)=c(H+)+c(HNO2),下列说法不正确的是( )
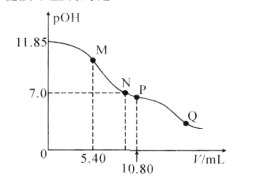
A.25°C时,HNO2电离常数的数量级是10-4
B.M点溶液中存在:2c(H+)+c(HNO2)=c(OH-)+c(NO2-)
C.图上M、N、P、Q四点溶液中所含离子的种类相同
D.a=10.80
【答案】B
【解析】
已知P点溶液中存在c(OH-)=c(H+)+c(HNO2),同时溶液中存在电荷守恒:c(OH-)+ c(NO2-)= c(H+)+ c(Na+),二式联立消去c(OH-)可得:c(NO2-)+ c(HNO2) =c(Na+),此为NaNO2溶液中的物料守恒式,即P点溶液中的溶质只有NaNO2,亚硝酸和氢氧化钠恰好完全反应,所以初始亚硝酸溶液的体积为10.80mL,据此分析作答。
A. HNO2电离常数K=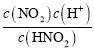 ,未滴加氢氧化钠时0.1mol/L的HNO2溶液的pOH=11.85,即溶液中c(OH-)=10-11.85mol/L,则根据水的电离平衡常数可知c(H+)=10-2.15mol/L,溶液中存在电离平衡HNO2H++NO2,溶液中氢离子浓度和亚硝酸根离子浓度大致相等,所以K=
,未滴加氢氧化钠时0.1mol/L的HNO2溶液的pOH=11.85,即溶液中c(OH-)=10-11.85mol/L,则根据水的电离平衡常数可知c(H+)=10-2.15mol/L,溶液中存在电离平衡HNO2H++NO2,溶液中氢离子浓度和亚硝酸根离子浓度大致相等,所以K=![]() ,故A正确;
,故A正确;
B. 根据分析可知a=10.80mL,所以当加入5.40mL氢氧化钠溶液时溶液中的溶质为等物质的量HNO2和NaNO2,存在电荷守恒:c(OH-)+ c(NO2-)= c(H+)+ c(Na+),存在物料守恒:c(NO2-)+ c(HNO2) =2c(Na+),二式联立可得2c(H+)+c(HNO2)=2c(OH-)+c(NO2-),故B错误;
C. M、N、P、Q四点溶液中均含有:H+、OH-、NO2-、Na+,故C正确;
D. 已知P点溶液中存在c(OH-)=c(H+)+c(HNO2),同时溶液中存在电荷守恒:c(OH-)+ c(NO2-)= c(H+)+ c(Na+),二式联立消去c(OH-)可得:c(NO2-)+ c(HNO2) =c(Na+),此为NaNO2溶液中的物料守恒式,即P点溶液中的溶质只有NaNO2,亚硝酸和氢氧化钠恰好完全反应,所以初始亚硝酸溶液的体积为10.80mL,故D正确;
故答案为B。


科目:高中化学 来源: 题型:
【题目】常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是
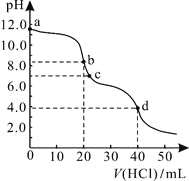
A. a点溶液呈碱性的原因用离子方程式表示为:CO![]() +2H2O
+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
B. c点处的溶液中c(Na+)-c(Cl-)=c(HCO![]() )+2c(CO
)+2c(CO![]() )
)
C. 滴定过程中使用甲基橙作为指示剂比酚酞更准确
D. d点处溶液中水电离出的c(H+)大于b点处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴的化合物在工业生产、生命科技等行业有重要应用。
(1)Co2+的核外电子排布式为___,Co的第四电离能比Fe的第四电离能要小得多,原因是___。
(2)Fe、Co均能与CO形成配合物,如Fe(CO)5、Co2(CO)8的结构如图1、图2所示,图1中1molFe(CO)5含有__mol配位键,图2中C原子的杂化方式为___,形成上述两种化合物的四种元素中电负性最大的是___(填元素符号)。
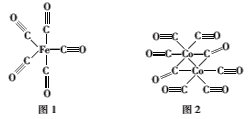
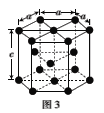
(3)金属钴的堆积方式为六方最密堆积,其配位数是___,钴晶体晶胞结构如图3所示,该晶胞中原子个数为___;该晶胞的边长为anm,高为cnm,该晶胞的密度为___(NA表示阿伏加德罗常数的值,列出代数式)g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用NaOH溶液来滴定邻苯二甲酸氢钾溶液有下列操作:
①向溶液中加入1~2滴指示剂
②取20.00 mL标准溶液放入锥形瓶中
③用NaOH溶液滴定至终点(终点时溶液的pH约为9.1)
④重复以上操作
⑤用天平精确称取一定量的邻苯二甲酸氢钾固体配成250 mL标准溶液(测得pH约为4.2)
⑥根据实验数据计算NaOH的物质的量浓度
(1)以上各步中,正确的(填序号)操作顺序是_____________________________,上述②中使用的仪器除锥形瓶外,还需要使用的仪器是______________。
(2)选用指示剂是______________,滴定终点现象______________________________________。
(3)滴定,并记录NaOH的终读数.重复滴定几次,数据记录如下表:
滴定次数实验数据 | 1 | 2 | 3 | 4 |
V(样品)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)/mL(初读数) | 0.10 | 0.30 | 0.00 | 0.20 |
V(NaOH)/mL(终读数) | 20.08 | 20.30 | 20.80 | 20.22 |
V(NaOH)/mL(消耗) | 19.98 | 20.00 | 20.80 | 20.02 |
某同学在处理数据过程中计算得到平均消耗NaOH溶液的体积为V(NaOH)=(19.98+20.00+20.80+20.02)/4mL=20.20mL,他的计算合理吗?理由是_______________。
(4)步骤②中在观察滴定管的起始读数时,要使滴定管的尖嘴部分充满溶液,滴定前用蒸馏水洗净碱式滴定管,然后加NaOH溶液进行滴定,此操作对实验结果________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在四个不同的容器中,在不同的条件下进行合成氨反应,根据下列在相同时间内测得的结果判断,生成氨的反应速率最快的是
A.v(NH3)=0.05 mol/(Lmin)B.v(NH3)=0.2 mol/(Lmin)
C.v(H2)=0.3 mol/(Lmin)D.v(H2)=0.4 mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把6 mol A气体和5 mol B气体混合充入4 L 密闭容器中,在一定条件下发生反应:3A(g)+B(g)![]() 2C(g)+xD(g),经5 s达到平衡,此时生成C为2 mol ,测得D的平均反应速率为0.1 mol·L-1·s-1,下列说法错误的是( )
2C(g)+xD(g),经5 s达到平衡,此时生成C为2 mol ,测得D的平均反应速率为0.1 mol·L-1·s-1,下列说法错误的是( )
A. x=2B. B的转化率为20%
C. 平衡时A的浓度为0.75 mol·L-1D. 恒温达到平衡时容器内的压强为开始的75%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是
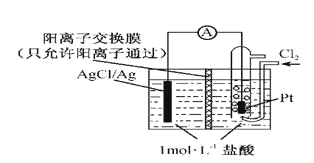
A. 正极反应为AgCl +e-=Ag +Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中。下列分析正确的()

A. K1闭合,铁棒上发生的反应为2H++2e-=H2↑
B. K1闭合,石墨棒周围溶液碱性增强
C. K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D. K2闭合,电路中通过0.002NA个电子时,两极共产生0.001mol气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积相同的两个密闭容器M和N中,保持温度为150 ℃,向M容器中加入a mol HI,同时向N容器中加入b mol HI (a>b)。当反应2HI(g)![]() H2 (g) + I2 (g) 达到平衡后,下列说法正确的是
H2 (g) + I2 (g) 达到平衡后,下列说法正确的是
A.从反应开始到达到平衡,所需时间tM > tN
B.平衡时cM(I2) = c N(I2)
C.平衡时I2 蒸气在混合气体中的体积分数:M > N
D.HI的平衡分解率αM = αN
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com