
【题目】下列各组物质,既能用酸性高锰酸钾溶液又能用溴水鉴别的是( )
A.戊烯和二甲苯B.乙烷和乙烯C.乙炔和乙烯D.苯和甲苯
科目:高中化学 来源: 题型:
【题目】生产措施与目的不相符的是
选项 | 生产措施 | 目的 |
A | 工业制硫酸:粉碎硫铁矿 | 提高反应的速率 |
B | 合成氨:铁触媒作催化剂 | 提高产物的产率 |
C | 海水提溴:热空气吹出Br2 | 提高Br2的纯度 |
D | 侯氏制碱:母液循环使用 | 提高原料利用率 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)9.8gH2SO4的物质的量是;2.0molH2O的质量是 .
(2)含Al3+5.4g的硫酸铝的物质的量为 , 其中含SO42﹣个.
(3)某二价金属1.6g在氧气中完全燃烧生成2g氧化物,则该金属的相对原子量 .
(4)6.02×1023个CO2与molH2质量相等,与gSO2含有的氧原子数相等.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某K2CO3样品中含有Na2CO3、KNO3和Ba(NO3)2三种杂质中的一种或两种,现将6.9g样品溶于足量水中,得到澄清溶液,若再加入过量的CaCl2溶液,得到4.5g沉淀,对样品所含杂质的正确判断是( )
A.肯定有KNO3和Na2CO3 , 没有Ba(NO3)2
B.肯定有KNO3 , 没有Ba(NO3)2 , 可能还有Na2CO3
C.肯定没有Na2CO3和Ba(NO3)2 , 可能有KNO3
D.以上判断都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中A~H均为中学化学中常见的物质,A、B、H是气体,它们之间有如图转化关系(反应中生成的水已略去). 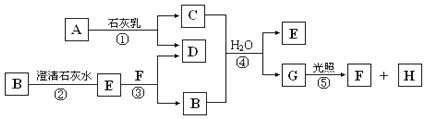
请回答以下问题:
(1)E是(填化学式),G是(填名称);
(2)C物质在日常生活中可作;
(3)写出反应①的化学方程式; C与浓盐酸反应,可以生成A气体,写出反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用标签所示浓盐酸配制250mL 0.4mol/L的稀盐酸,并进行有关实验. 
请回答:
(1)需要量取浓盐酸mL.
(2)配制该稀盐酸时使用的仪器除量筒、烧杯、玻璃棒外,还必须用到的仪器有、 .
(3)若实验遇到下列情况,所配溶液的浓度会(填“偏高”、“偏低”、“不变”) A、定容时仰视刻度线;
B、容量瓶内壁附有水珠而未干燥处理;
C、溶解后没有冷却便进行定容 .
(4)将所配制的稀盐酸倒入5.92g Na2CO3和NaHCO3的固体混合物中,恰好完全反应,则原混合物中Na2CO3的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某温度下,纯水的c(H+)=2×10- 7 mol·L-1,则此时c(OH-)为______;若温度不变,滴入稀盐酸使c(H+)=5×10- 4 mol·L-1则溶液中由水电离产生的c(H+)为______,此时温度______(填“高于”、“低于”或“等于”)25℃。
(2)已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ/mol
②H2(g)+![]() O2(g)===H2O(g) ΔH2=-242.0 kJ/mol
O2(g)===H2O(g) ΔH2=-242.0 kJ/mol
③CO(g)+![]() O2(g)===CO2(g) ΔH3=-283. 0 kJ/mol
O2(g)===CO2(g) ΔH3=-283. 0 kJ/mol
写出C(s)与水蒸气反应生成CO和H2的热化学方程式:
_________________________________________________。
(3)常温下,取物质的量浓度相同的NaOH和HCl溶液,以3∶2体积比相混合,所得混合液的pH=12,则原溶液的物质的量浓度为______。(溶液体积变化忽略不计)
(4)常温下,0.l mol·L-1 H3PO4溶液的pH小于7,括号内离子浓度的大小顺序为(H2PO4- 、HPO42- 、PO43- 、OH- 和H +)___________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验). 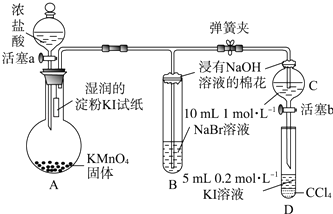
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸.
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a.
Ⅳ.…
(1)A中产生黄绿色气体,其电子式是 .
(2)验证氯气的氧化性强于碘的实验现象是 .
(3)B中溶液发生反应的离子方程式是 .
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是 .
(5)过程Ⅲ实验的目的是 .
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下 , 得电子能力逐渐减弱.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某恒容密闭容器中充入等物质的量的A 和B,一定温度下发生反应A(g)+xB(g)![]() 2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:

下列说法中正确的是
A. 30 min~40 min 之间该反应使用了催化剂
B. 反应方程式中的x=2,正反应为吸热反应
C. 30 min 时条件的变化是降低压强,40 min 时条件的变化是升高温度
D. 前20 min A 的平均反应速率为0.08 molL﹣1min﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com