
用如图所示装置除去含有CN﹣、Cl﹣废水中的CN﹣时,控制溶液pH为9~10,阳极产生的ClO﹣将CN﹣氧化为两种无污染的气体,下列说法不正确的是( )

A.用石墨作阳极,铁作阴极
B.阳极的电极反应式:Cl﹣+2OH﹣﹣2e﹣═ClO﹣+H2O
C.阴极的电极反应式:2H2O+2e﹣═H2↑+2OH﹣
D.除去CN﹣的反应:2CN﹣+5ClO﹣+2H + ═N2↑+2CO2↑+5Cl﹣+H2O
 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源:2015-2016学年吉林省松原市高一下期中化学试卷(解析版) 题型:选择题
下列事实可用勒夏特列原理解释的是
A.开启啤酒瓶后,瓶中立刻泛起大量泡沫
B.硫酸工业中,将黄铁矿粉碎后加入沸腾炉中
C.500℃左右比在室温时更有利于提高合成氨的转化率
D.对2HI  H2+I2平衡体系增加压强使颜色变深
H2+I2平衡体系增加压强使颜色变深
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二5月调研二化学试卷(解析版) 题型:填空题
某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振谱表明分子中只有一种类型的氢。该物质可发生如下转化,其中D1 、D2互为同分异构体,E1 、E2互为同分异构体。
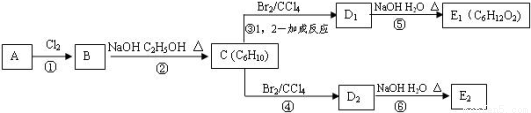
(1)A的名称为: C的结构简式为: ; E2含有的含氧官能团的名称为: 。
(2)反应②的化学方程式为: ,反应类型为: ; 反应⑥的化学方程式为: ,反应类型为: 。
(3)与A的分子式相同的烯烃,除A外还有 种不同的结构;写出其中主链为4个碳,分子中有三种不同类型的氢原子,且与A同类的所有物质的结构简式: (均不考虑立体异构) 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二5月调研二化学试卷(解析版) 题型:选择题
只用一种试剂,区别甲苯、四氯化碳、己烯、乙醇、碘化钾溶液、亚硫酸六种无色液体,应选用
A.酸性KMnO4溶液 B.碘水 C.溴水 D.硝酸银溶液
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前押题理综化学试卷(解析版) 题型:填空题
2015年2月16日李克强总理到东北调研经济情况,重点走访了钢铁厂,鼓励钢铁厂提高钢铁质量和产量,铁及其化合物在日常生活中应用广泛。
(1)利用Fe 2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理。已知含SO2的废气通入含Fe2+、Fe 3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4 H+ =4Fe3+ +2H2O,则另一反应的离子方程式为_________________;
(2)草酸亚铁为黄色固体,作为一种化工原料, 可广泛用于涂料、染料、陶瓷、玻璃器皿等的着色剂以及新型电池材料、感光材料的生产。合成草酸亚铁的流程如下:

①配制(NH4) 2Fe(SO4)2溶液时,需加入少量稀硫酸,目的是___________________。
②得到的草酸亚铁沉淀需充分洗涤,洗涤操作的具体方法为_________________________________,检验是否洗涤干净的方法是___________________________。
(3)将制得的产品(FeC2O4·2H2O)在氩气气氛中进行加热分解,结果如下图(TG%表示残留固体质量占原样品总质量的百分数)。
① 则A→B发生反应的化学方程式为:__________________________________。
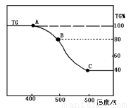
②已知 B→C过程中有等物质的量的两种气态氧化物生成,写出B→C的化学方程式____________;
(4)某草酸亚铁样品中含有少量草酸铵。为了测定不纯产品中草酸根的含量,某同学做了如下分析实验:
Ⅰ.准确称量m g 样品,溶于少量2mol/L 硫酸中并用 100mL 容量瓶定容。
Ⅱ.取上述溶液20mL,用c mol/L高锰酸钾标准溶液滴定,溶液变为淡紫色,消耗高锰酸钾溶液的体积为V 1 mL。
Ⅲ.向上述溶液中加入足量 Zn 粉,使溶液中的 Fe3+恰好全部还原为 Fe2+。
Ⅳ.过滤,洗涤剩余的锌粉和锥形瓶,洗涤液并入滤液
Ⅴ.用c mol/L KMnO4溶液滴定该滤液至溶液出现淡紫色,消耗KMnO4溶液的体积V 2 mL。
已知:2MnO4- +5H2C2O 4+6H+=2Mn2+ +10CO2+8H2O
MnO4- +8H++5Fe2+ =5Fe3+ + Mn2+ +4H2O
回答下列问题:
①若省略步骤Ⅳ,则测定的草酸根离子含量(填―偏大‖、―偏小‖或―不变‖)。
②mg样品中草酸根离子的物质的量为(用 c,V1,V2的式子表示,不必化简)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高二下第四次月考化学试卷(解析版) 题型:填空题
水处理技术在生产、生活中应用广泛,对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(1)水的净化和软化的区别是水的净化是用混凝剂将水中的胶体及悬浮物沉淀下来,而水的软化是______;
(2)生活用水必须保证安全,自来水厂需要对取自江河湖泊中的淡水进行杀菌消毒、混凝沉淀、过滤等工艺处理,这三项处理的正确顺序是___________________________;
(3)下列试剂能够用来对自来水进行杀菌消毒,且不会造成二次污染的是____(d____-填字母).
a.福尔马林 b.漂白粉 c.氯气 d.臭氧
(4)Na2FeO4是一种新型水处理剂,工业上可用FeSO4制备Na2FeO4其工艺流程如下:

①工业上常用硫酸亚铁作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加入绿矾.请解释这一做法的原因_________________________________(用必要的离子方程式和文字描述).
②写出由Fe(0H)3制取Na2FeO4的化学方程式_________________________________ ;
(5)石灰纯碱法是常用的硬水软化方法,已知25℃时Ksp(CaCO3)=2.8×10-9,现将等体积的Ca(OH)2溶液与Na2CO3溶液混合(假设溶液体积具有加和性),若Na2CO3溶液的浓度为5.6×10-5mol•L-1,则生成沉淀所需Ca(0H)2溶液的最小浓度为______________ 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高二下第四次月考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.0.1molCl2常温下与过量稀NaOH溶液反应转移电子总数为0.1NA
B.25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA
C.标准状况下,22.4LCHCl3含有的分子数为NA
D.1L 0.1mol•L-1的硫化钠溶液中硫离子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下第二次月考化学试卷(解析版) 题型:填空题
短周期元素P、Q、X、Y、Z原子序数逐渐增大。它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形。回答下列问题:
(1) Z的价电子排布式为____________,QZ3分子的空间构型为____________;
(2) X与Z构成的分子是_________分子(填“极性”或“非极性”)
(3) P和Y形成的化合物,其分子中包含__________键(填个数及 “σ键和π键”),该分子中P原子的杂化方式为____________,
(4) 写出一个验证Y与Z的非金属性强弱的离子反应方程式_________________;
(5) 金属镁在Q的单质中燃烧得到的产物与水反应生成两种碱性物质,该反应的化学方程式是____________________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州凯里一中高一下期中理科化学试卷(解析版) 题型:填空题
(1)元素周期表共有 个周期 个族;在周期表中有些族的元素还有些特别的名称,如第ⅠA族(除氢)___________;卤族元素属于第 族。
(2)2001年美国科学家宣布他们发现了核电荷数为116的元素,试推断该元素在元素周期表中的位置____________,若已知该元素原子核内有155个中子,则其质量数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com