
| A. | ①③⑥ | B. | ②④⑤ | C. | ①②⑦ | D. | ④⑤⑦ |
分析 由同种元素组成的不同单质为同素异形体,新型氧分子,它是由四个氧原子构成的(O4),互为同素异形体的应是氧元素组成的不同单质.
解答 解:新型氧分子,它是由四个氧原子构成的(O4),互为同素异形体的应是氧元素组成的不同单质,
①168O 是氧元素的一种原子,不是氧元素的同素异形体;
②O2是氧元素形成的单质和O4互为同素异形体;
③188O是氧元素的一种原子,不是氧元素的同素异形体;
④O3 是氧元素形成的单质和O4互为同素异形体
⑤O4是氧元素形成的单质和O2,O3 互为同素异形体;
⑥O2- 是氧元素形成的氧离子,不是氧元素的单质,不是同素异形体;
⑦O22-是过氧根离子,不是氧气的单质,不是同素异形体;
故互为同素异形体的是②④⑤;
故选B.
点评 本题考查了同素异形体概念的分析应用,注意概念实质理解应用,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| 选项 | 试剂 | 现象 | 结论 |
| A | 酸性KMnO4溶液 | 溶液褪色 | SO2有氧化性 |
| B | FeCl3溶液 | 溶液褪至浅绿色 | SO2有还原性 |
| C | 滴有酚酞的NaOH溶液 | 无明显变化 | SO2与NaOH溶液不反应 |
| D | 紫色石蕊试液 | 溶液变红后褪色 | SO2水溶液有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质与原子(或分子)结构 | |
| T | 最外层电子数是次外层电子数的3倍 | |
| X | 常温下单质为双原子分子,分子中含有3对共用电子对 | |
| Y | M层比K层少1个电子 | |
| Z | 第三周期元素的简单离子中半径最小 | |
| W | W带两个负电荷的阴离子与Ar具有相同电子层结构 | |
 .
.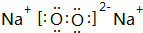 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
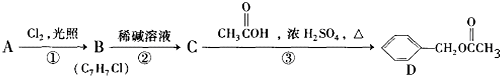
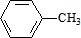 ,C的名称:苯甲醇
,C的名称:苯甲醇 +Cl2 $\stackrel{光照}{→}$
+Cl2 $\stackrel{光照}{→}$ 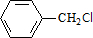 +HCl,取代反应
+HCl,取代反应 ,取代反应
,取代反应 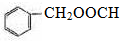 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
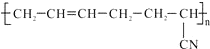 ,其具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )
,其具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )| A. | ①③⑤ | B. | ①③ | C. | ①④⑥ | D. | ④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol阿司匹林(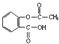 )与足量的NaOH溶液反应,消耗NaOH最大的物质的量为2mol )与足量的NaOH溶液反应,消耗NaOH最大的物质的量为2mol | |
| B. | 汽油、柴油等矿物油与植物油主要成分都是烃,均可以萃取溴水中的溴 | |
| C. | 丙氨酸和苯丙氨酸脱水,最多可生成4种二肽 | |
| D. | 苯酚能与溴水反应,苯不能与溴水反应,说明苯环对羟基有影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14C可用于文物年代的鉴定,14C与12C互为同素异形体 | |
| B. | 高空臭氧层吸收太阳紫外线,保护地球生物;低空过量臭氧是污染气体,对人体有害 | |
| C. | 光导纤维中所用材料为晶体硅 | |
| D. | NOx、SO2、CO2、PM2.5颗粒都会导致酸雨 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com