
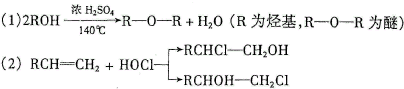

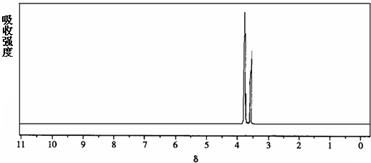
| 醇 |
| △ |
| 醇 |
| △ |


科目:高中化学 来源: 题型:
| A、由X与Y组成的化合物的沸点总低于由X与Z组成的化合物的沸点 |
| B、元素Z、W 的简单离子的电子层结构不同 |
| C、元素Y 的简单气态氢化物的热稳定性比Z 的强 |
| D、只含X、Y、Z 三种元素的化合物,可能是离子化合物,也可能是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol乙烷中的氢原子被氯原子完全取代,需要氯气分子数为 4 NA |
| B、1 mol的NO2 与水完全反应转移电子数为NA |
| C、在标准状况下2.24 L O2 和3.2 g O3含有氧原子都为0.2 NA. |
| D、在标准状况下2.24 L丙烷和戊烷混合物含分子个数为0.1 NA. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 研究目的 | 压强对反应的影响 | 温度对反应的影响 | 增加O2浓度对反应的影响 | 浓度对平衡常数的影响 |
| 图示 | 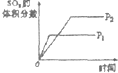 |  | 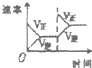 |  |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
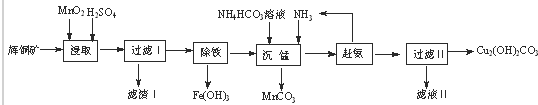
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28g |
| B、常温下,1L0.1mol.L-1的NH4NO3溶液中NH4+和NO3-总数为0.2NA |
| C、标准状况下,4.48 L重水(D20)含有的中子数为2NA |
| D、1 mol甲基(-CH3)所含电子数为9NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
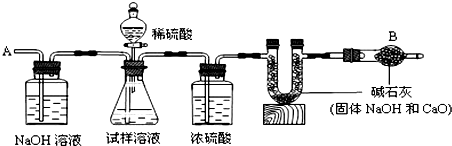
查看答案和解析>>
科目:高中化学 来源: 题型:
A、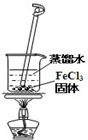 该实验:搅拌,溶液显黄色,即配得氯化铁溶液 |
B、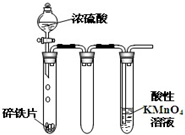 该实验:铁片最终完全溶解,且高锰酸钾溶液变无色 |
C、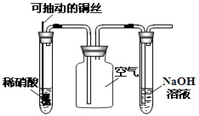 该实验:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内产生红棕色气体 |
D、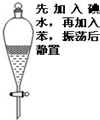 该实验:溶液分层,上层溶液变为紫色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com