
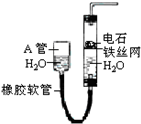
 如图中的实验装置,可用于制取乙炔,请填写下列空白:
如图中的实验装置,可用于制取乙炔,请填写下列空白: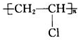 .
. 分析 图示装置可通过调节A管的高度,控制反应的发生和停止:将A管提高,右管中水面上升,与电石接触发生反应;将A管降低,右管中水面下降,水与电石脱离接触,反应停止,则制取乙炔的化学反应方程式为CaC2+2H2O→Ca(OH)2+CH≡CH↑,乙炔含有C≡C键,可发生加成、加聚和氧化反应.
(1)通过调节A管液面可以控制右管中液面,从而控制反应的发生与停止;
(2)实验室通过碳化钙(电石)与水的反应制取乙炔;
(3)有机物含碳量越高,燃烧火焰越明亮,烟越浓;
(4)乙炔与氯化氢发生加成反应生成氯乙烯,氯乙烯加成聚合生成聚氯乙烯.
解答 解:(1)有图可知:将A管提高,右管中水面上升,与电石接触发生反应;将A管降低,右管中水面下降,水与电石脱离接触,反应停止,所以通过调节A管液面高度以控制反应的发生和停止;
故答案为:调节水面高度以控制反应的发生和停止;
(2)实验室用碳化钙和水反应制取乙炔,反应的化学反应方程式为:CaC2+2H2O→Ca(OH)2+CH≡CH↑,
故答案为:CaC2+2H2O→Ca(OH)2+CH≡CH↑;
(3)乙炔中含碳的质量分数较大,燃烧时火焰明亮并伴有浓烈的黑烟,
故答案为:火焰明亮伴有浓烈的黑烟;
(4)乙炔与氯化氢发生加成反应生成氯乙烯,氯乙烯加成聚合生成聚氯乙烯,化学方程式为:CH≡CH+HCl→CH2=CHCl,nCH2=CHCl$\stackrel{引发剂}{→}$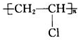 ;
;
故答案为:CH≡CH+HCl→CH2=CHCl,nCH2=CHCl$\stackrel{引发剂}{→}$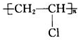 .
.
点评 本题考查乙炔的实验室制法及其性质,侧重基础知识的考查,有利于培养学生的分析能力和实验能力,注意相关基础知识的积累,难度中等.


科目:高中化学 来源: 题型:推断题
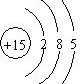 .
.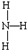 .X在纯氧中燃烧的产物无毒无污染,该反应的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
.X在纯氧中燃烧的产物无毒无污染,该反应的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L H2O含有分子数为NA | |
| B. | 分子总数为NA的N2气体体积约为22.4 L | |
| C. | 常温常压下,1.6 g CH4含分子数为0.1NA | |
| D. | 常温常压下,3.2g氧气所含氧原子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据金属失去电子的多少来判断,失去电子较多的金属性较强 | |
| B. | 用钠置换MgCl2溶液中的Mg2+,来验证钠的金属性强于Mg | |
| C. | Mg不与NaOH溶液反应而Al能与NaOH溶液反应,可说明金属性:Al>Mg | |
| D. | 碱性:NaOH>Mg(OH)2>Al(OH)3,可说明钠、镁、铝金属性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 弱电解质的电离是一个吸热的过程 | |
| B. | 化学反应中的能量变化不仅仅表现为热量变化 | |
| C. | 反应物的总能量大于生成物的总能量的反应是吸热反应 | |
| D. | 断裂化学键吸收能量,形成化学键放出能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
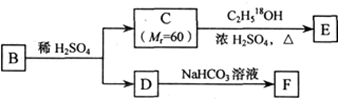
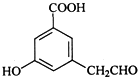 、
、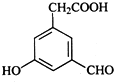 .
.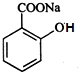 ;
;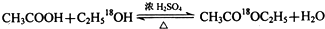 ②D与浓溴水反应
②D与浓溴水反应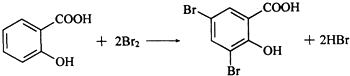
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16g甲烷所含有的电子数是8NA | |
| B. | 常温常压下,4g氦气所含有的原子数目为NA | |
| C. | 标准状况下,1L己烷充分燃烧后生成CO2分子数为3/11.2 NA | |
| D. | 常温常压下,1mol丙烷所含有的共价键数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
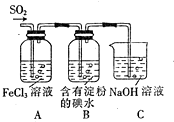
| A. | SO42-是SO2气体与Fe3+反应的还原产物 | |
| B. | 装置C烧杯中加入少量苯可以防止倒吸 | |
| C. | 表明I-的还原性弱于SO2的现象是B中溶液蓝色褪色 | |
| D. | 在A中的溶液加入KMnO4溶液,则紫红色褪去说明A中SO2与Fe3+发生了氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com