
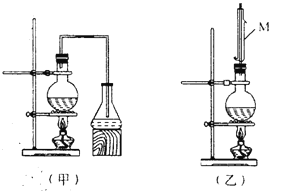
【题目】实验室制取乙酸丁酯的实验装置有以下甲、乙两种装置可供选用。
制备乙酸丁酯所涉及的有关物质的物理性质见下表:
乙酸 | 1-丁醇 | 乙酸丁酯 | |
熔点(℃) | 16.6 | -89.5 | -73.5 |
沸点(℃) | 117.9 | 117 | 126.3 |
密度(g/cm3) | 1.05 | 0.81 | 0.88 |
水溶性 | 互溶 | 可溶(9g/100g水) | 微溶 |
(1)仪器M的名称为_________。
(2)制取乙酸丁酯选用乙装置而不选用甲装置的理由是__________。
(3)从制备乙酸丁酯所得的混合物中分离、提纯乙酸丁酯时,需要经过多步操作,下列图示的操作中,肯定需要的化学操作是______(选填答案编号)。
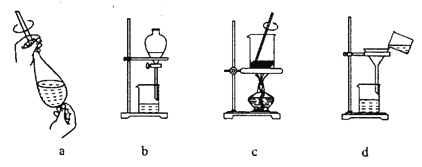
(4)有机物的分离操作中,经常需要使用分液漏斗等仪器。使用分液漏斗前必须_____(填写操作)。某同学在进行分液操作时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还可能_________(写出一点)。
【答案】 直形冷凝管 由于乙酸、1-丁醇的沸点低于乙酸丁酯的沸点,若采用甲装置,会造成反应物的大量挥发,降低了反应物的转化率,乙装置含有冷凝回流装置,可以冷凝回流反应物,提高反应物的转化率,所以选乙装置。 ab 检查是否漏水 分液漏斗上口玻璃塞未打开
【解析】(1)根据仪器构造可判断仪器M的名称为直形冷凝管;(2)由于反应物乙酸、1-丁醇的沸点低于产物乙酸丁酯的沸点,若采用甲装置,会造成反应物的大量挥发,降低了反应物的转化率,乙装置含有冷凝回流装置,可以冷凝回流反应物,提高反应物的转化率,所以选乙装置。(3)从制备乙酸丁酯所得的混合物中分离、提纯乙酸丁酯时,首先要萃取,然后分液即可,答案选ab。(4)使用分液漏斗前必须检查是否漏水或堵塞。若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还可能是分液漏斗上口玻璃塞未打开(或漏斗内部未与大气相通,或玻璃塞上的凹槽未与漏斗口上的小孔对准)。


科目:高中化学 来源: 题型:
【题目】〔化学——选修3:物质结构与性质〕举世瞩目的中国探月工程三期再入返回试验器于2014年10月24日凌晨成功发射,为实现月球采样和首次地月往返踏出了成功的第一步。探月工程三期的主要目标是实现无人自动采样返回,突破月面采样、月面上升、月球轨道交会对接等核心关键技术。已知所用火箭推进剂为肼(N2H4)和过氧化氢(H2O2),火箭箭体一般采用钛合金材料。
请回答下列问题:
(1)N2H4、H2O2分子中电负性最大的元素在周期表中的位置为 ,第一电离能最大的元素为 。
(2)钛的原子序数为22,其基态电子排布式示意图为 。
(3)1 mol N2H4分子中含有的键数目为 。
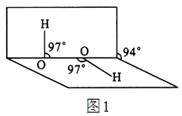
(4)H2O2分子结构如图1,其中心原子杂化轨道为 ,估计它难溶于CS2,简要说明原因 。
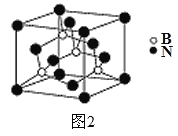
(5)氮化硼其晶胞如图2所示,则处于晶胞顶点上的原子的配位数为 ,若立方氮化硼的密度为g·cm-3,阿伏加德罗常数为NA,则两个最近N原子间的距离为________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁铝合金因坚硬、轻巧、美观、易于加工而成为被广泛应用的新型建筑装潢材料,主要用于制作窗框、卷帘门、防护栏等。下列与这些用途无关的性质是
A. 不易生锈 B. 导电性好
C. 密度较小 D. 强度较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲是一种盐,由A、B、C、D、E五种短周期元素元素组成。甲溶于水后可电离出三种离子,其中含有由A、B形成的10电子阳离子。A元素原子核内质子数比E的少1,D、E处于同主族。用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
③取少量甲溶液于试管中,向其中加入稀盐酸,再加入BaCl2溶液,出现白色沉淀;
③取少量甲溶液于试管中逐滴滴入NaOH溶液,生成沉淀的质量与滴入NaOH溶液的体积关系如下图所示,

④取少量甲溶液于试管中,加入过最的NaOH溶液并加热。
回答下列问题:
(1)C的元素符号是_______,D在周期表中的位置是________。
(2)经测定甲晶体的摩尔质量为453 gmol-1,其中阳离子和阴离子物质的量之比为1:1,则甲晶体的化学式为________。
(3)实验③中根据图象得V(oa):V(ab):V(bc)= _______。
(4)实验④中离子方程式是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,其中Z为金属且Z的原子序数为W的2倍。n、p、q是由这些元素组成的二元化合物,常温下n为气体。m、r、s分别是Z、W、X的单质,t的水溶液显碱性且焰色反应呈黄色,上述物质间的转化关系如图所示。下列说法正确的是
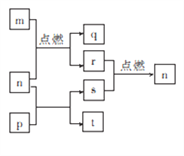
A. 原子半径:Z>Y
B. 化合物p中只存在离子键
C. 图示转化关系涉及的反应均为氧化还原反应
D. 最简单气态氢化物的稳定性:W>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜的配合物A结构如图图1。请回答下列问题:
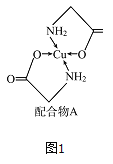
(1)写出基态Cu的外围电子排布式________
(2)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中σ键和x键数目之比是___;N2O与CO2互为等电子体,则N2O的电子式为_______。
(3)在Cu催化下,甲醇可被氧化为甲醛,甲醇分子中HCO的键角____(选填“大于”、“等于”或“小于”) l20°;甲醛能与水形成氢健,请在如图2中表示出来____。
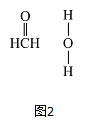
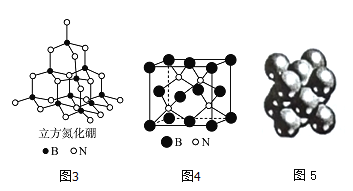
(4)立方氮化硼如图3、图4与金刚石结构相似,是超硬材料。立方氮化硼晶体内B一N键数与硼原子数之比为__________;
(5)Cu晶体的堆积方式如图5所示,设Cu原子半径为a,晶体中Cu原子的配位数为_____,晶体的空间利用率为_________。(已知:![]() ,列式并计算出结果)
,列式并计算出结果)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期非金属主族元素X、Y、Z、W的原子序数依次增大。在如图所示物质转化关系中,l是由该四种元素组成的离子化合物,m是Y的单质,n是Z的单质,p是W的单质,其余为由上述的两种或三种元素组成的化合物。u的水溶液具有漂白性;常温时,0.01mol·L-1t与0.01mol·L-1 v溶液的pH均为2。
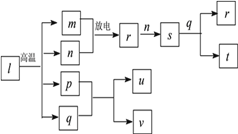
请回答:
(1)X、Y、Z的原子半径由大到小的顺序为____。
(2)l高温分解时,破坏的微粒间作用力有____。
(3)在l中W显最高价,则l溶液肯定显____性,用离子方程式表示其原因____。
(4)s+q→r+t反应中,若消耗了s 13.8g,则转移的电子数目为____。
(5)X和Y形成的常见化合物为YX3。YX3遇到p会有白烟产生,写出可能的化学方程式__。请设计实验方案检验该白烟的成分____。
(6)化合物YX2ZX的水溶液呈弱碱性,室温下,其电离常数Kb=9.0×10-9,0.10 mol·L-1该物质的溶液中c(H+)为_____ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化剂的叙述中,正确的是
A. 组成氧化剂的每一种元素在反应中都获得电子
B. 氧化剂中至少有一种元素的化合价在反应中降低
C. 氧化剂中至少有一种元素的化合价在反应中升高
D. 同一化学反应中氧化剂和还原剂不可能是同一种物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com