
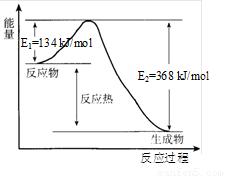
在400℃、101kPa时,NO2(g)+CO(g)=NO(g)+CO2(g)反应过程的能量变化如下图所示。下列说法不正确的是
A. 该反应是放热反应
B. 该反应的反应热△H =-234 kJ/mol
C. 加入催化剂,使该反应的活化能降低,反应速率加快,同时使该反应的反应热数值减小
D. 由图可推出:NO(g)+CO2(g)NO2(g)+CO(g)△H=+234 kJ/mol
科目:高中化学 来源: 题型:
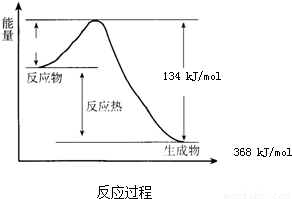
 在400℃、101kPa时,NO2(g)+CO(g)?NO(g)+CO2(g)反应过程的能量变化如图所示.
在400℃、101kPa时,NO2(g)+CO(g)?NO(g)+CO2(g)反应过程的能量变化如图所示.查看答案和解析>>
科目:高中化学 来源:2013届北京市高二下学期期中考试化学试卷(解析版) 题型:选择题
在400℃、101kPa时,NO2(g)+CO(g)=NO(g)+CO2(g)反应过程的能量变化如下图所示。下列说法不正确的是
A. 该反应是放热反应
B. 该反应的反应热△H =-234 kJ/mol
C. 加入催化剂,使该反应的活化能降低,反应速率加快,同时使该反应的反应热数值减小
D. 由图可推出:NO(g)+CO2(g) NO2(g)+CO(g)△H
=+234 kJ/mol
NO2(g)+CO(g)△H
=+234 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2011-2012学年北京市门头沟区育园中学高二(下)期末化学试卷(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com