
【题目】如右图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中。下列分析正确的()

A. K1闭合,铁棒上发生的反应为2H++2e-=H2↑
B. K1闭合,石墨棒周围溶液碱性增强
C. K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D. K2闭合,电路中通过0.002NA个电子时,两极共产生0.001mol气体
【答案】B
【解析】A、K1闭合构成原电池,铁是活泼的金属,铁棒是负极,铁失去电子,铁棒上发生的反应为Fe+2e-=Fe2+,A不正确;B、K1闭合构成原电池,铁棒是负极,铁失去电子,石墨棒是正极,溶液中的氧气得到电子转化为OH-,电极反应式为O2+4e-+2H2O=40H-,石墨棒周围溶液pH逐渐升高,B正确;C、K2闭合构成电解池,铁棒与电源的负极相连,作阴极,溶液的氢离子放电产生氢气,铁不会被腐蚀,属于外加电流的阴极保护法,C不正确;D、K2闭合构成电解池,铁棒与电源的负极相连,作阴极,溶液中的氢离子放电生成氢气。石墨棒是阳极,溶液中的氯离子放电生成氯气,电极反应式分别为2H++2e-=H2↑、2Cl--2e-=Cl2↑,电路中通过0.002NA个电子时,两极均产生0.001mol气体,共计是0.002mol气体,D不正确,答案选B。
点晴:本题通过电解饱和氯化钠溶液为载体,重点考查原电池和电解池的判断,金属的腐蚀与防护以及电极产物判断和计算,意在考查学生分析问题、解决问题的能力。熟练掌握电化学原理,准确判断正、负极以及阴、阳极,明确两极的电极反应及电池反应是解题的关键。该类试题的难点在于是电极反应式的书写和有关计算。


科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A. 配制FeCl2溶液时,加入铁粉的原因:Fe+Fe3+=2Fe2+
B. 二氧化锰和浓盐酸反应:MnO2+4HCl(浓)![]() Mn2++2Cl2↑+2H2O
Mn2++2Cl2↑+2H2O
C. “水玻璃”长期暴露在空气中会变质:SiO32-+CO2+H2O=H2SiO3↓+CO32-
D. 向硫酸氢钠溶液中滴加氢氧化钡溶液至中性:H++SO42++Ba2++OH-=BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表是元素周期表的一部分,请回答有关问题:
主族 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | VⅡA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素是 . (用元素符号表示)
(2)②③④三种元素的原子半径从大到小的顺序是 (用元素符号表示)
(3)用电子式表示③与⑦形成化合物的过程 .
(4)在①~⑧元素中,元素的最高价氧化物对应的水化物中碱性最强的 . (填化学式)
(5)在⑦与⑩的单质中,化学性质较活泼的是(填化学式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NH3催化还原氮的氧化物,可以消除氮的氧化物的污染。已知:
反应①:4NH3(g)+ 6NO(g)![]() 5N2(g) + 6H2O(l) △H1
5N2(g) + 6H2O(l) △H1
反应②:2NO(g) + O2(g)![]() 2NO2(g) △H2(△H2<0且
2NO2(g) △H2(△H2<0且![]() )
)
反应③:4NH3(g) + 6NO2(g)![]() 5N2(g)+ 3O2 + 6H2O(l) △H3
5N2(g)+ 3O2 + 6H2O(l) △H3
反应①和反应②在不同温度时的平衡常数及其大小关心如下表:
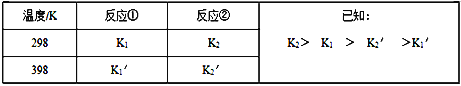
(1)试推测反应③是______ 反应(填“吸热”或“放热”)
(2)相同条件下反应①在2L的密闭容器中选用不同的催化剂,反应产生N2的物质的量随时间的变化如图所示。

则:
①计算0~4min时在A催化剂作用下,反应速率v(NO)=__________。
②下列说法正确的是:__________________。
A.该反应的活化能大小顺序是:Ea(A)>Ea(B) >Ea(C)
B.增大压强能使反应速率加快的原因,是因为增加活化分子的百分数
C.单位时间内H-O键与N-H断裂的数目相等时,说明反应已达平衡状态
D.若在恒容绝热的密闭容器中进行,当温度不变时,说明反应已达平衡状态
(3)对于反应②,若在某温度下,在容积为2L的刚性密闭容器中起始加入2 molNO和2 molO2,反应一段时间后,测的生成NO21.6mol,则该反应是否达到平衡状态?_______(填“是”或“不是”。已知该温度下该反应的K约为147.3)。达平衡后,在同一温度下向大小相同的另一刚性容器中加入1.2mol的NO2和0.9mol的O2,则还要加入NO______mol、O2_____mol,达平衡时各物质的浓度才能跟前平衡的相等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如右图。下列有关氢氧燃料电池的说法不正确的是

A. 该装置将化学能转化为电能
B. 为了增加灯泡亮度,可以将电极碳棒变得粗糙多孔
C. 电子迁移方向:电极a→灯泡→电极b→电解质溶液→电极a
D. 该电池的总反应:2H2+O2=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 2H2S+SO2=3S↓+2H2O中,氧化产物和还原产物物质的量之比为2:1
B. 4Zn+10HNO3=4Zn(NO3)2+NH4NO3+3H2O中,氧化剂和还原剂物质的量之比为5:2
C. 3I2+6KOH![]() 5KI+KIO3+3H2O中,被氧化和被还原的碘原子物质的量之比为1:5
5KI+KIO3+3H2O中,被氧化和被还原的碘原子物质的量之比为1:5
D. 2FeS+6H2SO4(浓)![]() Fe2(SO4)3+3SO2↑+2S↓+6H2O中,发生氧化反应和发生还原反应的硫原子物质的量之比为2:3
Fe2(SO4)3+3SO2↑+2S↓+6H2O中,发生氧化反应和发生还原反应的硫原子物质的量之比为2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示的直型石英玻璃封管中充有CO气体,左端放置不纯的镍(Ni)粉。在一定条件下,Ni可以与CO(g)发生如下反应: ,但Ni粉中的杂质不与CO(g)发生反应。玻璃管内左右两端的温度分别稳定在350 K和470 K,经过足够长时间后,右端的主要物质是
,但Ni粉中的杂质不与CO(g)发生反应。玻璃管内左右两端的温度分别稳定在350 K和470 K,经过足够长时间后,右端的主要物质是

A. 纯Ni(s)和Ni(CO)4(g) B. 纯Ni(s)和CO(g)
C. 不纯Ni(s)和CO(g) D. 不纯Ni(s)和Ni(CO)4(g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com