
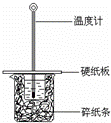
某同学按照课本实验要求,用50mL 0.50mol•L﹣1的盐酸与50mL 0.55mol•L﹣1的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应 过程中所放出的热量计算中和热.下列说法中,正确的是( )
A.实验过程中没有热量损失
B.图中实验装置缺少环形玻璃搅拌棒
C.烧杯间填满碎纸条的作用是固定小烧杯
D.若烧杯上不盖硬纸板,测得的△H将偏小
考点:中和热的测定.
分析:A.根据实验过程的保温情况确定保温效果;
B.根据量热计的构造来判断该装置的缺少仪器;
C.根据烧杯间填满碎纸条的作用是保温;
D.根据大烧杯上不盖硬纸板,热量容易散失.
解答: 解:A.该装置的保温效果并不如量热计那样好,大小烧杯之间要填满纸片,装置存在热量的散失,故A错误;
B.根据量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒,故B正确;
C.中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失,故C错误;
D.大烧杯上不盖硬纸板,热量容易散失,中和热的数值偏小,但中和热△H会偏大,故D错误;
故选:B.
点评:本题考查学生有关中和热测定原理,可以根据所学知识进行回答,注意比较中和热大小时要考虑“﹣“号.


科目:高中化学 来源: 题型:
下列有关物质的性质与应用均正确的是( )
A. SO2和Cl2都能使品红溶液褪色,两者等体积混合可以增强漂白能力
B. Na2O2是碱性氧化物,具有强氧化性可用于杀菌消毒
C. 氨气是一种碱性气体,可用碱石灰或无水CaCl2干燥
D. MgO的熔点很高,可用于制作耐高温材料
查看答案和解析>>
科目:高中化学 来源: 题型:
青苹果汁遇碘溶液显蓝色,熟苹果汁能还原银氨溶液,这说明( )
A.青苹果中只含淀粉不含糖类 B.熟苹果中只含糖类不含淀粉
C.苹果转熟时淀粉水解为单糖 D.苹果转熟时单糖聚合成淀粉
查看答案和解析>>
科目:高中化学 来源: 题型:
有四种常见药物①阿司匹林②青霉素③胃舒平④麻黄碱.请回答:
(1)某同学胃酸过多,应选用的药物是 (填序号).
(2)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是 (填序号).
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是 (填序号).
(4)滥用药物会导致不良后果,如过量服用 (填序号)会出现水杨酸中毒,应立即停药,并静脉注射NaHCO3.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学平衡常数K的说法中,正确的是( )
A.K的大小与起始浓度有关
B.温度越高,K值越大
C.K值越大,反应物的转化率越大
D.K值越大,正向反应进行的程度越小
查看答案和解析>>
科目:高中化学 来源: 题型:
高温下,某反应达到平衡,平衡常数K=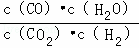 .恒容时,温度升高,H2浓度减小.下列说法正确的是( )
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应的化学方程式为CO+H2O CO2+H2
CO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,H2(g)+CO2(g)⇌H2O(g)+CO(g) 的平衡常数K=2.25.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示.下列判断不正确的是( )

A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看答案和解析>>
科目:高中化学 来源: 题型:
若以w1和w2分别表示物质的量是浓度为c1 mol/L和c2 mol/L氨水溶液的质量分数,已知2w1=w2,则下列推断正确的是( )(已知氨水的密度小于纯水的密度)
A.2c1=c2 B.2c2=c1 C.c2>2c1 D.c1<c2<2c1
查看答案和解析>>
科目:高中化学 来源: 题型:
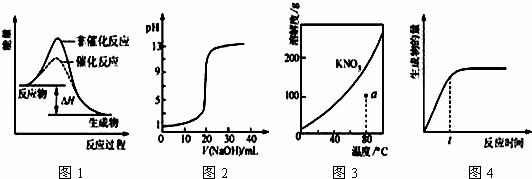
下列图示与对应的叙述相符的是( )
|
| A. | 图1表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
|
| B. | 图2表示0.1000 mol•L﹣1NaOH溶液滴定20.00mL0.1000 mol•L﹣1CH3COOH溶液所得到的滴定曲线 |
|
| C. | 图3表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 |
|
| D. | 图4表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时v逆>v正 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com