
分析 (1)过氧化钠与二氧化碳反应生成碳酸钠和氧气,可以做供氧剂;
(2)硅酸钠与二氧化碳、水反应生成碳酸钠和硅酸;
(3)①氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水;
②漂白粉有效成分为次氯酸钙,次氯酸钙与盐酸反应生成氯化钙、氯气和水,依据氯元素化合价变化计算转移电子数,判断被氧化的氯化氢物质的量.
解答 解:(1)过氧化钠与二氧化碳反应生成碳酸钠和氧气,方程式:2Na2O2+2CO2=2Na2CO3+O2;
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(2)硅酸钠与二氧化碳、水反应生成碳酸钠和硅酸,离子方程式:SiO32-+H2O+CO2=H2SiO3↓+CO32-;
故答案为:SiO32-+H2O+CO2=H2SiO3↓+CO32-;
(3)①氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,离子方程式:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
②漂白粉有效成分为次氯酸钙,化学式Ca(ClO)2,次氯酸钙与盐酸反应生成氯化钙、氯气和水,化学方程式:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O,依据方程式可知:生成1mol氯气,有2mol氯化氢被氧化,转移2mol电子,则产生3.36L氯气(标准状况),物质的量为$\frac{3.36L}{22.4L/mol}$=0.15mol,转移0.3mol电子,有0.3mol氯化氢被氧化;
故答案为:Ca(ClO)2; Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O;0.3mol;0.3mol.
点评 本题考查了化学方程式的书写,明确相关物质的性质及发生反应实质是解题关键,注意氧化还原反应基本概念与规律的应用,题目难度中等.


 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔质量:mol/g | B. | 物质量:mol | ||
| C. | 溶解度:g/100g | D. | 气体摩尔体积:L/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 方法 | 选用试剂 | 现象 |
| 第一种(萃取) | 氯水、四氯化碳 | 下层溶液显紫色 |
| 第二种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
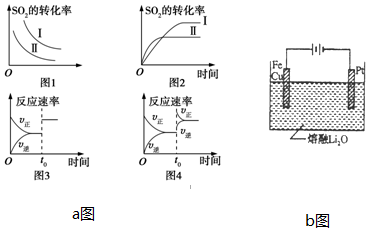
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ③⑤⑥ | C. | ①②③④⑤ | D. | ①②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +5、4 | B. | +5、7 | C. | +5、5 | D. | +7、7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu做还原剂 | B. | H2做氧化剂 | ||
| C. | 铜元素的化合价降低 | D. | 铜是氧化产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com