

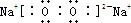 ,B为NH3,为三角锥形结构,
,B为NH3,为三角锥形结构,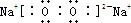 ;三角锥形;
;三角锥形;
| ||
| ||
| 4.48L |
| 22.4L/mol |
| 0.2mol |
| 0.1L |


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量NaOH固体样品,溶入水中,再滴加 | NaOH已变质 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量NaOH固体样品,溶于水中,再加入 | 该瓶NaOH已全部变质 | |
| 在上述滤液中滴加 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H4 |
| B、C2H2 |
| C、C3H6 |
| D、C6H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溴单质常温下为液态,但极容易挥发为溴蒸气 |
| B、溴单质只具有氧化性 |
| C、溴原子外层有7个电子,在化学反应中容易得1个电子,表现氧化性 |
| D、溴离子可以用酸性AgNO3溶液来检验 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com