
”¾ĢāÄæ”æĻĀĮŠŹżĮæµÄĪļÖŹÖŠŗ¬¶ŌÓ¦Ī¢Į£ŹżÄæ×ī¶ąµÄŹĒ
A”¢0£®4molNaClĖłŗ¬Ąė×ÓŹż
B”¢±ź×¼×“æöĻĀ5£®6L CO2Ėłŗ¬Ō×ÓŹż
C”¢1L1 mol”¤L£1ŃĪĖįĖłŗ¬HCl·Ö×ÓŹż
D”¢10gÄŹĘųĖłŗ¬Ō×ÓŹż
”¾“š°ø”æA
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗA”¢0£®4molNaClĖłŗ¬Ąė×ÓŹżŹĒ0£®8NA; B”¢±ź×¼×“æöĻĀ5£®6L CO2Ėłŗ¬Ō×ÓŹżŹĒ(5£®6L”Ā22£®4L/mol)”Į3 NA=0£®75 NA; C”¢HClŹĒĒæµē½āÖŹ£¬ŌŚĖ®ÖŠĶźČ«µēĄė£¬ĖłŅŌ1L1 mol”¤L£1ŃĪĖįĖłŗ¬HCl·Ö×ÓŹżŹĒ0£»D”¢ÄŹĘųŹĒµ„Ō×Ó·Ö×Ó¹¹³ÉµÄĪļÖŹ£¬10gÄŹĘųĖłŗ¬Ō×ÓŹż(10g”Ā20g/mol) ”Į NA=0£®5 NA;ĖłŅŌŗ¬ÓŠµÄĪ¢Į£×ī¶ąµÄŹĒ0£®8NA;Ń”ĻīŹĒA”£


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹ŲÓŚČŻĮæĘæµÄŹ¹ÓĆ£¬ĻĀĮŠ²Ł×÷ÕżČ·µÄŹĒ( )
A. Ź¹ÓĆĒ°²»ÓĆ¼ģŃéČŻĮæĘæŹĒ·ńĀ©Ņŗ
B. ÓĆÕōĮóĖ®Ļ“µÓŗó±ŲŠėŅŖ½«ČŻĮæĘæŗęøÉ
C. ĪŖĮĖ±ćÓŚ²Ł×÷£¬ÅØČÜŅŗĻ”ŹĶ»ņ¹ĢĢåČܽāæÉÖ±½ÓŌŚČŻĮæĘæÖŠ½ųŠŠ
D. ĪŖĮĖŹ¹ĖłÅäČÜŅŗÅØ¶Č¾łŌČ£¬¶ØČŻ½įŹųŗó£¬ŅŖŅ”ŌČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹ²»ŹōÓŚÓŠ»śĪļµÄŹĒ£Ø £©
A. “×Ėį B. Ēč»ÆÄĘ(NaCN) C. ÓĶĖį(C17H33COOH) D. ±ūČż“¼
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµŖ»ÆĀĮ£ØAIN£¬ÓöĖ®Ņ×Ė®½ā£©¹ć·ŗÓ¦ÓĆÓŚ¼Æ³ÉµēĀ·Éś²śĮģÓņ”£Ä³ŃŠ¾æŠ”×éĄūÓƵŖĘų”¢Ńõ»ÆĀĮŗĶ»īŠŌĢæÖĘČ”µŖ»ÆĀĮ£¬Éč¼ĘČēĶ¼1ĖłŹ¾ŹµŃé×°ÖĆ”£
Ēė»Ų“š£ŗ
£Ø1£©Ķ¼1ÖŠÓƱ„ŗĶNaNO2ČÜŅŗÓėNH4ClČÜŅŗ¼ÓČČÖĘČ”µŖĘų£¬øĆ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø2£©Ķ¼1×°ÖĆÖŠø÷ŅĒĘ÷µ¼¹ÜæŚĮ¬½ÓµÄĖ³ŠņŹĒ(ÓĆŠ”Š“×ÖÄøa”śgĢīŠ“)£ŗ £»µ¼¹ÜAµÄ×÷ÓĆŹĒ ”£
£Ø3£©°“£Ø2£©Į¬½ÓŗĆŹµŃé×°ÖĆŗ󣬽ÓĻĀĄ“µÄ²Ł×÷ŹĒ ”£
£Ø4£©°“£Ø2£©Į¬½ÓµÄŹµŃé×°ÖĆ“ęŌŚµÄȱĻŻŹĒ ”£
£Ø5£©·“Ó¦½įŹųŗó£¬Ä³Ķ¬Ń§ÓĆĶ¼2×°ÖĆ½ųŠŠŹµŃ饓²ā¶Ø µŖ»ÆĀĮѳʷµÄÖŹĮæ·ÖŹż£ØŹµŃéÖŠµ¼¹ÜĢå»żŗöĀŌ²»¼Ę£©”£
¢ŁµŖ»ÆĀĮÓė¹żĮæµÄNaOHČÜŅŗ·“Ӧɜ³É°±Ęų»Æѧ·“Ó¦·½³ĢŹ½ĪŖ £»
¢Ś ¼ÆĘųĘæÖŠµÄ±½µÄ×÷ÓĆŹĒ £»¼ÆĘųĘæÖŠµÄŅŗĢåƻӊװĀś£¬ŌņŹµŃé²āµĆNH3µÄĢå»ż½« £ØĢī”°Ę«“ó”±”¢”°Ę«Š””±”¢”°²»±ä”±£©”£
¢ŪČōŹµŃéÖŠ³ĘČ”µŖ»ÆĀĮѳʷµÄÖŹĮæĪŖ10.0 g£¬²āµĆ°±ĘųµÄĢå»ż3. 36 L£Ø±ź×¼×“æö£©£¬Ōņѳʷ֊AlNµÄÖŹĮæ·ÖŹżĪŖ £Ø±£Įō3Ī»ÓŠŠ§Źż×Ö£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ·“Ó¦£ŗ¢Ł![]() £¬¢Ś
£¬¢Ś![]() £¬¢Ū
£¬¢Ū![]() £¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. ÉĻŹöČżøö·“Ó¦¶¼ÓŠµ„ÖŹÉś³É£¬ĖłŅŌ¶¼ŹĒÖĆ»»·“Ó¦
B. Ńõ»ÆŠŌÓÉĒæµ½ČõĖ³ŠņĪŖ![]()
C. ·“Ó¦¢ŚÖŠ»¹Ō¼ĮÓėŃõ»Æ¼ĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ6:1
D. ¢ŪÖŠ![]() »¹Ō¼Į·“Ó¦ŌņŃõ»Æ¼ĮµĆµ½µē×ÓµÄĪļÖŹµÄĮæĪŖ
»¹Ō¼Į·“Ó¦ŌņŃõ»Æ¼ĮµĆµ½µē×ÓµÄĪļÖŹµÄĮæĪŖ![]()
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææÕ¼äŹµŃéŹŅ”°Ģģ¹¬Ņ»ŗÅ”±µÄ¹©µēĻµĶ³ÖŠÓŠŌŁÉśĒāŃõČ¼ĮĻµē³Ų(RFC)£¬RFCŹĒŅ»ÖÖ½«Ė®µē½ā¼¼ŹõÓėĒāŃõČ¼ĮĻµē³Ų¼¼ŹõĻą½įŗĻµÄæɳäµēµē³Ų”£ĻĀĶ¼ĪŖRFC¹¤×÷ŌĄķŹ¾ŅāĶ¼£¬ÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
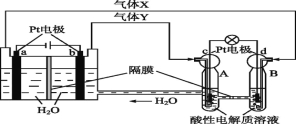
A£®µ±ÓŠ0.1 molµē×Ó×ŖŅĘŹ±£¬a¼«²śÉś1.12 L O2(±ź×¼×“æöĻĀ)
B£®b¼«ÉĻ·¢ÉśµÄµē¼«·“Ó¦ŹĒ£ŗ4H2O+4e- =2H2”ü+4OH-
C£®c¼«ÉĻ½ųŠŠ»¹Ō·“Ó¦£¬BÖŠµÄH+æÉŅŌĶعżøōĤ½ųČėA
D£®d¼«ÉĻ·¢ÉśµÄµē¼«·“Ó¦ŹĒ£ŗO2+4H++4e- =2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»¶ØĪĀ¶ČĻĀµÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬µ±ĻĀĮŠÄÄŠ©Įæ²»ŌŁ·¢Éś±ä»ÆŹ±£¬±ķĆ÷ĻĀŹö·“Ó¦£ŗ
A£Øs£©£«2B£Øg£©![]() C£Øg£©£«D£Øg£©ŅŃ“ļµ½Ę½ŗāדĢ¬£ŗ
C£Øg£©£«D£Øg£©ŅŃ“ļµ½Ę½ŗāדĢ¬£ŗ
¢Ł»ģŗĻĘųĢåµÄŃ¹Ēæ ¢Ś»ģŗĻĘųĢåµÄĆܶČ
¢ŪBµÄĪļÖŹµÄĮæÅØ¶Č¢ÜĘųĢåµÄ×ÜĪļÖŹµÄĮæ
¢Ż»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ
¢ŽĪļÖŹCµÄ°Ł·Öŗ¬Įæ ¢ßø÷ĘųĢåµÄĪļÖŹµÄĮæ
¢ąµ±ÓŠ1molBĘųĢå·Ö×Ó¶Ļ¼ü£¬Ķ¬Ź±ÓŠ1/2molCĘųĢå·Ö×Ó¶Ļ¼ü
A£®¢Ś¢Ū¢Ż¢Ž¢ß¢ą B£®¢Ł¢Ś¢Ū¢Ž¢ß¢ą C£®¢Ś¢Ū¢Ü¢Ż¢Ž¢ą D£®¢Ł¢Ū¢Ü¢Ż¢ß
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĀĮĶĮæóµÄÖ÷ŅŖ³É·ÖĪŖŃõ»ÆĀĮ”¢Ńõ»ÆĢśŗĶ¶žŃõ»Æ¹č£¬¹¤ŅµÉĻ¾¹żĻĀĮŠ¹¤ŅÕæÉŅŌŅ±Į¶½šŹōĀĮ£ŗ
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
ĻĀĮŠĖµ·ØÖŠ“ķĪóµÄŹĒ( )
A£®¢Ł¢ŚÖŠ³ż¼ÓŹŌ¼ĮĶā£¬»¹ŠčŅŖ½ųŠŠ¹żĀĖ²Ł×÷
B£®a”¢bÖŠĀĮŌŖĖŲµÄ»ÆŗĻ¼ŪĻąĶ¬
C£®¢ŪÖŠŠčŅŖĶØČė¹żĮæµÄ°±Ęų
D£®¢Ü½ųŠŠµÄ²Ł×÷ŹĒ¼ÓČČ£¬¶ųĒŅdŅ»¶ØŹĒŃõ»ÆĀĮ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®Ä¦¶ūŹĒ¹ś¼ŹæĘѧ½ē½ØŅé²ÉÓƵÄŅ»ÖÖĪļĄķĮæ
B£®HNO3µÄĦ¶ūÖŹĮæŹĒ63g
C£®ĪŅĆĒ°Ńŗ¬ÓŠ6.02”Į1023øöĮ£×ÓµÄČĪŗĪĮ£×ӵļÆĢå¼ĘĮæĪŖ1Ħ¶ū
D£®1molŃõŗ¬6.02”Į1023øöO2
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com