(1)取一定量的铁粉与2mol?L
-1稀硝酸400mL反应,反应后硝酸和铁均无剩余(铁只显+2价),且硝酸的还原产物只有NO.(不考虑溶液体积的变化)
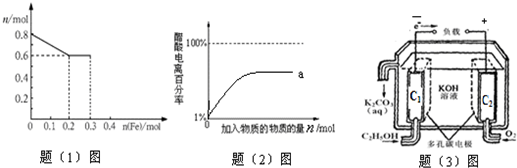
①若将铁粉慢慢加入到稀硝酸中,并搅拌,反应过程中溶液里Fe
3+、H
+、NO
3ˉ 三种离子中的某离子的物质的量的变化曲线如下图(1)所示,则该曲线表示的是
物质的量变化.
②若下图(1)中,当反应消耗0.2mol铁时,所需时间为2分钟,则H
+离子的反应速率为
.
(2)0.10mol?L
-1的稀醋酸中存在着平衡:CH
3COOH?CH
3COOˉ+H
+.
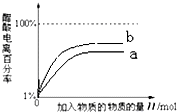
①在图(2)中a表示向稀醋酸中不断加水,b表示向稀醋酸中慢慢滴加0.10mol?Lˉ
1的稀氢氧化钠溶液.a中醋酸电离百分率的变化图线已画出,请你在上左图(1)中画出b过程中醋酸电离百分率的变化图线.
②一定温度下,利用pH计测定不同浓度醋酸溶液的pH值,得到如下数据:
| 醋酸浓度(mol?L-1) | 1 | 0.1 | 0.01 |
| pH值 | 2.50 | 3.00 | 3.50 |
求该温度下醋酸的电离常数
.当醋酸浓度为0.1mol?L
-1时,则电离百分率为
.
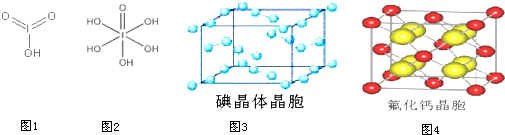
(3)乙醇是一种可再生能源,可用它来制成燃料电池(如上图3),试写出其负极的电极反应式
.现用该燃料电池为电源,实现在铁片上镀铜,应将
与铁片相连,当铁片上镀上19.2g铜时,消耗的乙醇为
克.


 ,故答案为:
,故答案为: ;
;

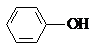 和
和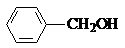 互为同系物
互为同系物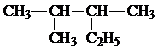 的名称为2-甲基-3-乙基丁烷
的名称为2-甲基-3-乙基丁烷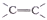 ⑥-C6H5 ⑦Br-⑧-COOH 其中不是官能团的是( )
⑥-C6H5 ⑦Br-⑧-COOH 其中不是官能团的是( )