
分析 A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次递增.A原子核内仅有1个质子,则A为氢元素;D原子的最外层电子数是次外层电子数的3倍,最外层电子数不超过8,原子只能有2个电子层,最外层电子数为6,故D为氧元素;B原子的电子总数与D原子的最外层电子数相等,则B为碳元素;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等,则C原子最外层电子数为1+4=5,其原子序数小于氧,故C为氮元素.
解答 解:A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次递增.A原子核内仅有1个质子,则A为氢元素,元素符号为H;D原子的最外层电子数是次外层电子数的3倍,最外层电子数不超过8,原子只能有2个电子层,最外层电子数为6,故D为氧元素,元素符号为O;B原子的电子总数与D原子的最外层电子数相等,则B为碳元素,元素符号为C;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等,则C原子最外层电子数为1+4=5,其原子序数小于氧,故C为氮元素,元素符号为N,
故答案为:氢,H;碳,C; 氮,N;氧,O.
点评 本题考查结构与位置关系,关键是熟练掌握短周期元素,理解掌握核外电子排布规律,有利于基础知识的巩固.


科目:高中化学 来源: 题型:选择题
| A. | 元素X、W的简单阴离子具有相同的电子层结构 | |
| B. | W的简单气态氢化物的热稳定性比Y的强 | |
| C. | 由Y、Z两种元素组成的化合物是离子化合物 | |
| D. | 原子半径:r(X)<r(Y)<r(Z)<r(W) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1×(10-14+10-10)mol•L-1 | B. | $\frac{1×{(10}^{-14}{+10}^{-10})}{2}$mol•L-1 | ||
| C. | 2×10-10mol•L-1 | D. | 2×10-14mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 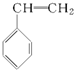 | B. | 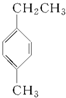 | C. | 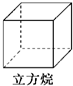 | D. | 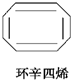 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 双键、三键中一定含有π键 | |
| B. | 成键原子间原子轨道重叠越多,共价键越牢固 | |
| C. | 因每个原子未成对电子数是一定的,故配对原子个数也一定 | |
| D. | 每一个原子轨道在空间都具有方向性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑦ | B. | ①②③⑦ | C. | ①⑦ | D. | ②④⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | - |
| 最低价态 | - | - | -2 | - | -4 | -3 | -1 | - | -3 | -1 |
 或
或 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在水中溶解性:Na2CO3<NaHCO3 | |
| B. | 热稳定性:Na2CO3<NaHCO3 | |
| C. | 同浓度溶液与足量酸反应产生气体的速度:Na2CO3<NaHCO3 | |
| D. | Na2CO3不能转化成NaHCO3,而NaHCO3能转化为Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅胶可作袋装食品的干燥剂 | |
| B. | 用活性炭可除去冰箱中的异味 | |
| C. | CO2、NO2、或SO2都会导致酸雨的形成 | |
| D. | 大量燃烧化石燃料是造成雾霾天气的一种重要因素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com