
| ĪĀ¶Č”ę | 25 | 80 | 230 |
| Ę½ŗā³£ŹżÖµ | 5”Į104 | 2 | 1.9”Į10-5 |
| A£® | ÉĻŹö·“Ó¦ŹĒģŲŌö·“Ó¦ | |
| B£® | 25”ꏱ£¬·“Ó¦G£Øg£©?E£Øs£©+4F£Øg£©µÄĘ½ŗā³£ŹżÖµŹĒ0.5 | |
| C£® | ŌŚ80”ꏱ£¬²āµĆijŹ±æĢ£¬F”¢GÅØ¶Č¾łĪŖ0.5 mol•L-1£¬Ōņ“ĖŹ±v£ØÕż£©£¾v£ØÄę£© | |
| D£® | ŗćĪĀŗćČŻĻĀ£¬ĻņČŻĘ÷ÖŠŌŁ³äČėÉŁĮæG£Øg£©£¬“ļŠĀĘ½ŗāŹ±£¬GµÄĢå»ż°Ł·Öŗ¬Į潫Ōö“ó |
·ÖĪö A£®Õż·“Ó¦ĪŖĘųĢåĪļÖŹµÄĮæ¼õŠ”µÄ·“Ó¦£¬Õż·“Ó¦ĪŖģŲ¼õµÄ·“Ó¦£»
B£®ĻąĶ¬ĪĀ¶ČĻĀ£¬G£Øg£©?E£Øs£©+4F£Øg£©µÄĘ½ŗā³£ŹżÓėE£Øs£©+4F£Øg£©?G£Øg£©µÄĘ½ŗā³£Źż»„ĪŖµ¹Źż£»
C£®¼ĘĖć“ĖŹ±ÅضČÉĢQc£¬ČōQc=K£¬“¦ÓŚĘ½ŗāדĢ¬£¬ČōQc£¼K£¬·“Ó¦ĻņÕż·“Ó¦½ųŠŠ£¬ČōQc£¾K£¬·“Ó¦ĻņÄę·“Ó¦½ųŠŠ£¬½ų¶ųČ·¶Øv£ØÕż£©”¢v£ØÄę£©µÄĻą¶Ō“󊔣»
D£®ŗćĪĀŗćČŻĻĀ£¬ĻņČŻĘ÷ÖŠŌŁ³äČėÉŁĮæG£Øg£©£¬Ļą¶ŌĪŖŌŚŌĘ½ŗā»ł“”ÉĻŌö“óŃ¹Ēæ£¬Ę½ŗāÕżĻņŅĘ¶Æ£®
½ā“š ½ā£ŗA£®Õż·“Ó¦ĪŖĘųĢåĪļÖŹµÄĮæ¼õŠ”µÄ·“Ó¦£¬Õż·“Ó¦ĪŖģŲ¼õµÄ·“Ó¦£¬¹ŹA“ķĪó£»
B£®ĻąĶ¬ĪĀ¶ČĻĀ£¬G£Øg£©?E£Øs£©+4F£Øg£©µÄĘ½ŗā³£ŹżÓėE£Øs£©+4F£Øg£©?G£Øg£©µÄĘ½ŗā³£Źż»„ĪŖµ¹Źż£¬¹Ź25”ꏱ£¬·“Ó¦G£Øg£©?E£Øs£©+4F£Øg£©µÄĘ½ŗā³£ŹżÖµŹĒ$\frac{1}{5”Į1{0}^{4}}$=2”Į10-5£¬¹ŹB“ķĪó£»
C£®“ĖŹ±ÅضČÉĢQc=$\frac{0.5}{0£®{5}^{4}}$=8£¾K=2£¬·“Ó¦ĻņÄę·“Ó¦½ųŠŠ£¬¹Źv£ØÕż£©£¼v£ØÄę£©£¬¹ŹC“ķĪó£»
D£®ŗćĪĀŗćČŻĻĀ£¬ĻņČŻĘ÷ÖŠŌŁ³äČėÉŁĮæG£Øg£©£¬Ļą¶ŌĪŖŌŚŌĘ½ŗā»ł“”ÉĻŌö“óŃ¹Ēæ£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬“ļŠĀĘ½ŗāŹ±£¬GµÄĢå»ż°Ł·Öŗ¬Į潫Ōö“󣬹ŹDÕżČ·£¬
¹ŹŃ”£ŗD£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāÓ°ĻģŅņĖŲ”¢»ÆŃ§Ę½ŗā³£ŹżÓ¦ÓĆµČ£¬×¢Ņā¶ŌĘ½ŗā³£ŹżµÄĄķ½ā£¬ÕĘĪÕ»ÆŃ§Ę½ŗā³£ŹżµÄÓĆĶ¾£ŗ1”¢ÅŠ¶Ļ·“Ó¦½ųŠŠµÄ³Ģ¶Č£¬2”¢ÅŠ¶Ļ·“Ó¦µÄČČŠ§Ó¦£¬3”¢ÅŠ¶Ļ·“Ó¦½ųŠŠµÄ·½Ļņ£¬4”¢¼ĘĖć×Ŗ»ÆĀŹµČ£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ö×ÓŹ½ĪŖC2H6OµÄÓŠ»ś»ÆŗĻĪļŠŌÖŹĻąĶ¬ | |
| B£® | ĻąĶ¬Ģõ¼žĻĀ£¬µČÖŹĮæµÄĢ¼°“a”¢bĮ½ÖÖĶ¾¾¶ĶźČ«×Ŗ»Æ£¬Ķ¾¾¶a±ČĶ¾¾¶b·Å³öøü¶ąČČÄÜ Ķ¾¾¶a£ŗC$”ś_{øßĪĀ}^{H_{2}O}$CO+H2$”ś_{Č¼ÉÕ}^{O_{2}}$CO2+H2O Ķ¾¾¶b£ŗC$”ś_{Č¼ÉÕ}^{O_{2}}$CO2 | |
| C£® | Ź³ĪļÖŠæɼÓČėŹŹĮæµÄŹ³Ę·Ģķ¼Ó¼Į£¬ČēĻć³¦ÖŠæÉŅŌ¼ÓÉŁĮæµÄŃĒĻõĖįÄĘŅŌ±£³ÖČāÖŹŠĀĻŹ | |
| D£® | ÉśŹÆ»Ņ”¢Ģś·Ū”¢¹č½ŗŹĒŹ³Ę·°ü×°ÖŠ³£ÓƵÄøÉŌļ¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŠņŗÅ | ¼× | ŅŅ |
| ¢Ł | SO2 | ŹÆ»ŅĖ® |
| ¢Ś | CO2 | ŹÆ»ŅĖ® |
| ¢Ū | SO2 | Ba£ØNO3£©2 |
| ¢Ü | NO2 | CaCl2 |
| A£® | ¢Ś¢Ū¢Ü | B£® | ¢Ś¢Ū | C£® | ¢Ł¢Ū¢Ü | D£® | ¢Ł¢Ś¢Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
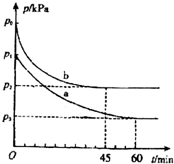 Įņ¼°Ęä»ÆŗĻĪļ¶ŌČĖĄąµÄÉś²śŗĶÉś»īÓŠ×ÅÖŲŅŖµÄ×÷ÓĆ£®
Įņ¼°Ęä»ÆŗĻĪļ¶ŌČĖĄąµÄÉś²śŗĶÉś»īÓŠ×ÅÖŲŅŖµÄ×÷ÓĆ£®| ŹµŃ鱹ŗÅ | ĪĀ¶Č | ĘšŹ¼Ź±ĪļÖŹµÄĮæ/mol | Ę½ŗāŹ±ĪļÖŹµÄĮæ/mol | |
| N£ØSO2£© | N£ØNO2£© | N£ØNO£© | ||
| ¼× | T1 | 0.80 | 0.20 | 0.18 |
| ŅŅ | T2 | 0.20 | 0.80 | 0.16 |
| ±ū | T3 | 0.20 | 0.30 | a |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
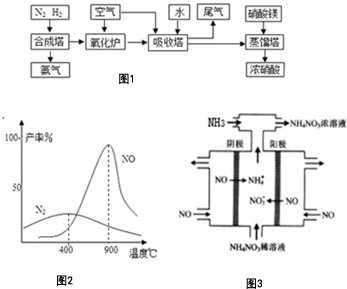 °±”¢ĻõĖį”¢ĻõĖįļ§”¢ĻõĖįĶŹĒÖŲŅŖµÄ»Æ¹¤²śĘ·£®¹¤ŅµŗĻ³É°±ÓėÖʱøĻõĖįŅ»°ćæÉĮ¬ŠųÉś²ś£¬Į÷³ĢČēĶ¼1£ŗĒė»Ų“šĻĀĮŠĪŹĢā
°±”¢ĻõĖį”¢ĻõĖįļ§”¢ĻõĖįĶŹĒÖŲŅŖµÄ»Æ¹¤²śĘ·£®¹¤ŅµŗĻ³É°±ÓėÖʱøĻõĖįŅ»°ćæÉĮ¬ŠųÉś²ś£¬Į÷³ĢČēĶ¼1£ŗĒė»Ų“šĻĀĮŠĪŹĢā²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
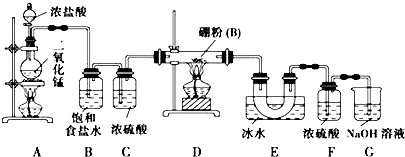
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
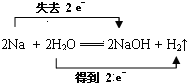 ·“Ó¦ÖŠ£¬H2OŹĒŃõ»Æ¼Į£®
·“Ó¦ÖŠ£¬H2OŹĒŃõ»Æ¼Į£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com