
【题目】某市售盐酸试剂瓶标签上的部分信息如下:
盐酸
分子式:HCl
相对分子质量:36.5
密度约1.18 g·mL-1
HCl的质量分数:36.5%
(1)该盐酸的物质的量浓度c(HCl)=__ mol·L-1。
(2)取该盐酸50 mL加水稀释到500 mL,则稀释后溶液中(HCl)= ___mol·L-1。
(3)取稀释后盐酸溶液100mL,该溶液中所含的氯离子的个数为:N(Cl—)=___NA
(4)取稀释后的适量盐酸与足量的锌粒作用,生成0.25 mol氢气,在标准状况下气体的体积是___L。
【答案】11.8 1.18 0.118 5.6
【解析】
(1)依据c=![]() 计算盐酸的物质的量浓度;
计算盐酸的物质的量浓度;
(2)依据稀释过程中溶质的物质的量不变计算稀释后盐酸浓度;
(3)依据n=cV和N=n NA计算;
(4)依据V=nVm计算。
(1)该盐酸的物质的量浓度c=![]() =
=![]() =11.8mol/L,故答案为:11.8;
=11.8mol/L,故答案为:11.8;
(2)设稀释后盐酸浓度为c,则依据稀释过程中溶质的物质的量不变得:11.8mol/L×50mL=500mL×c,解得c=1.18mol/L,故答案为:1.18;
(3)稀释后100mL盐酸中含有氯离子的物质的量为0.1L×1.18mol/L=0.118mol,数目为0.118 NA,故答案为:0.118;
(4)0.25mol氢气在标准状况下的体积是0.25mol×22.4L/mol=5.6L,故答案为:5.6。


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
【题目】明矾[KAl(SO4)2·12H2O]是一复盐,在造纸等方面应用广泛。某兴趣小组采用10.0g废易拉罐(含90%的Al,还含有少量的Fe、Mg等杂质)制备明矾的实验方案如下:
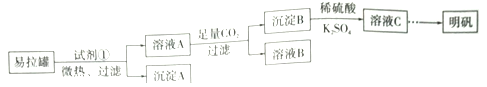
(1)试剂①应选用_____________(填代号)。
a.盐酸 b.H2SO4溶液 c.氯化钠溶液 d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为____________________。
(3)溶液B中溶质的主要成分为____________________ (填化学式)。
(4)从溶液C中得到明矾的实验操作步骤为蒸发浓缩、__________(填操作名称)、过滤、洗涤、干燥。如下图所示,蒸发操作中的一处错误是_____________。

(5)该小组在实验完成之后,得到118.5 g明矾,则明矾的回收率为_____________。(已知:明矾的摩尔质量为474g·mol-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.60g二氧化硅晶体中含有2NA个硅氧键
B.18g氨基(—ND2)中含有的电子数为9NA
C.80 °C时,lLpH =1的硫酸溶液中,含有的OH—数目为10—13NA
D.氯碱工业中,导线上流过NA个电子,则阳极放出氯气11.2 L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列说法正确的是( )
A.含有相同铜原子数的Cu2S和CuO的质量相等B.2g氢气所含质子数目为NA
C.lmol氨气含有的原子数目为2NAD.22.4LCH4所含电子数目为l0NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】世界能源消费依靠化学技术,作为燃料的H2通常来自水煤气。回答下列问题:
(1)己知:① C(s)+H2O(g)=CO(g)+H2(g)△H=akJ/mol②2C(s)+O2(g)=2CO(g) △H= -220 kJ/mol③2H2O(g)=2H2(g)+O2(g) △H=+480 kJ/mol,则 a=_____kJ/mol。
(2)某实验小组在实验室模拟反应C(s) +H2O (g)![]() CO (g) +H2 (g)能够说明该反应达到平衡状态的是____。
CO (g) +H2 (g)能够说明该反应达到平衡状态的是____。
a. v逆(H2O)=v正(CO) b.容器中物质的总质量不发生变化
c. n (H2O):n (H2)=1:1且不再改变 d.恒容容器中混合气体密度不变
(3)一定温度下,在2L盛有足量炭粉的恒容密闭容器中通入0.8molH2O发生反应①,6min时生成0.7 gH2则6 min内以CO表示的平均反应速率为 ______mol/Lmin-1 (保留2位有效数字)。
(4)燃料气中CO需氧化为CO2与氢气进行分离,使用CuO/CeO2做催化剂,并向其中加入不同的酸(HIO3 或H3PO4)后,CO的转化率随温度的变化如图所示。
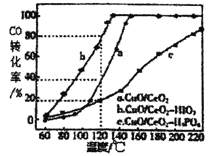
①加入H3PO4__________(填“促进”或,抑制”)CuO/CeO2的催化。
②CeO2可由草酸鋪[Ce2(C2O4)3]在空气中灼烧制备,同时只产生一种气体,写出该反应的化学方程式_____。
③恒温恒压下,在温度为120°C,催化剂为CuO/CeO2HIO3条件下反应,若起始时燃料气流速为1800mLmin-1,其中CO的体积分数为0.68%,则反应0.5h后剩余气体中CO的体积为__mL。
(5)有人将合成氨反应设计成原电池,装置如图所示。
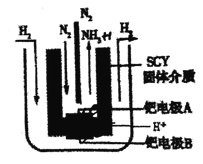
①正极反应式为 _______。
②己知该原电池的标准电动势![]() ,25°C时反应的平衡常数K与
,25°C时反应的平衡常数K与![]() 之间的关系为
之间的关系为![]() (n为原电池反应转移的电子数),则合成氨反应(N2 +3H2
(n为原电池反应转移的电子数),则合成氨反应(N2 +3H2![]() 2NH3)的平衡常数K为 ______(用含a的代数式表示,不需要化简)。
2NH3)的平衡常数K为 ______(用含a的代数式表示,不需要化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物I是一种医药合成中间体,实验室以芳香烃A为原料制备I的路线如下(部分反应条件已省略):
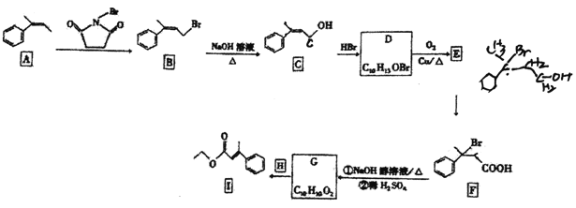
已知:RCH=CH2+HBr![]() RCH2CH2Br。回答下列问题:
RCH2CH2Br。回答下列问题:
(1)X的分子式为C8H8,且X与A互为同系物,则X的化学名称是 ______。
(2)B生成C的反应类型是_____, B、C含有的相同的官能团名称是 _____。
(3)碳原子上连有4个不同原子或基团时,该碳原子为手性碳原子。写出D的结构简式,并用星号![]() 标出其中的手性碳原子_____。
标出其中的手性碳原子_____。
(4)写出D—E 的化学反应方程式:_________。
(5)G的结构简式是 ______。
(6)Y与C是同分异构体,Y中含苯环,且苯环上有2个取代基,Y能发生银镜反应,其核磁共振氢谱中有5组峰,且峰面积之比为6:2:2:1:1,则Y的结构简式为 _______。
(7)丙二酸(HOOCCH2COOH)主要用作医药合成中间体、电镀抛光剂等。结合题目信息,设计以丙烯(CH3CH=CH2) 和![]() 为原料制备丙二酸的合成路线______(无机试剂任选)。
为原料制备丙二酸的合成路线______(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,![]() 和
和![]() 的电离常数分别为
的电离常数分别为![]() 和
和![]() 。将
。将![]() 和体积均相同的两种酸溶液分别稀释,其
和体积均相同的两种酸溶液分别稀释,其![]() 随加水体积的变化如图所示。下列叙述正确的是( )
随加水体积的变化如图所示。下列叙述正确的是( )

A. 曲线Ⅰ代表![]() 溶液
溶液
B. 溶液中水的电离程度:b点>c点
C. 从c点到d点,溶液中 保持不变(其中
保持不变(其中![]() 、
、![]() 分别代表相应的酸和酸根离子)
分别代表相应的酸和酸根离子)
D. 相同体积a点的两溶液分别与![]() 恰好中和后,溶液中
恰好中和后,溶液中![]() 相同
相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种用于驱动检验管道焊缝设备爬行器的甲醇-燃料电池的工作原理示意如图,下列有关该电池说法正确的是
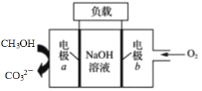
A.该电池工作时,每消耗22.4 L CH3OH转移6 mol电子
B.电子由电极a经负载流向电极b,再经过氢氧化钠溶液返回电极a,形成闭合回路
C.电池工作时,OH-向电极a移动,溶液的pH减小
D.电极b上发生的电极反应为O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据原电池原理,回答下列问题:

(1)图1是依据氧化还原反应:Cu(s)+2Fe3+(aq)=Cu2+(aq)+2Fe2+(aq)设计的原电池装置。
①电极X的材料是________(填化学名称);电极Y的材料是__________(填化学名称)。
②Y电极发生的电极反应式为:______________。
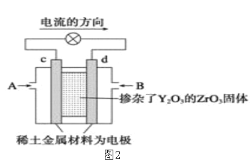
(2)图2是使用固体电解质的燃料电池,装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导正极生成的O2-离子(O2+4e―→2O2-)。
①c电极为______________极。(填“正”或“负”)
②d电极上的电极反应式为___________________________。
③如果消耗甲烷160g,假设化学能完全转化为电能,则转移电子的数目为______________(用NA表示),需要消耗标准状况下氧气的体积为_______L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com