
【题目】由下列实验及现象不能推出相应结论的是
实验 | 现象 | 结论 | |
A | 向2 mL 0.1mol/L的FeCl3溶液中加足量铁粉,振荡,加2滴KSCN溶液 | 黄色逐渐消失,加KSCN溶液颜色不变 | 还原性:Fe>Fe2+ |
B | 在稀AgNO3溶液中先加入足量0.1mol/L NaCl溶液,再加入少量0.1mol/L NaI溶液 | 先产生白色沉淀,后出现黄色沉淀 | 说明Ksp(AgCl)>Ksp(AgI) |
C | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 石蕊试纸变蓝 | NH4HCO3显碱性 |
D | 常温下,测定等物质的量浓度的Na2CO3和Na2SO4溶液的pH值 | 前者的 pH值比后者的大 | 非金属性:S>C |
A. AB. BC. CD. D
【答案】C
【解析】
A. 向2 mL 0.1mol/L的FeCl3溶液中加足量铁粉,发生反应:2Fe3++Fe=3Fe2+,反应中Fe为还原剂,Fe2+为还原产物,所以还原性Fe>Fe2+,可观察到黄色逐渐消失,加KSCN溶液颜色不变,A正确;
B.在稀AgNO3溶液中先加入足量0.1mol/L NaCl溶液,发生反应:Ag++Cl-=AgCl↓,产生白色沉淀,由于NaCl过量,所以Ag+反应完全,再加入少量0.1mol/L NaI溶液,出现黄色沉淀,说明发生反应:AgCl(s)+I-(aq)![]() AgI (s)+ Cl-(aq),说明物质的溶解度AgCl>AgI,由于二者的构型相同,则Ksp(AgCl)>Ksp(AgI),B正确;
AgI (s)+ Cl-(aq),说明物质的溶解度AgCl>AgI,由于二者的构型相同,则Ksp(AgCl)>Ksp(AgI),B正确;
C.加热盛有少量NH4HCO3固体的试管,NH4HCO3受热发生分解反应,产生NH3、CO2、H2O,NH3是碱性气体,遇到湿润的红色石蕊试纸,NH3与水反应产生NH3H2O,NH3H2O是一元弱碱,电离产生OH-,使试纸变为蓝色,因此不能证明NH4HCO3显碱性,C错误;
D.碳酸、硫酸是C、S最高价含氧酸,Na2CO3和Na2SO4是碳酸、硫酸的钠盐,元素的非金属性越强,其最高价含氧酸的酸性越强,由于NaOH是强碱,等物质的量浓度的Na2CO3和Na2SO4溶液的pH值,前者大,说明是强碱弱酸盐,显碱性,后者是强酸强碱盐,溶液显中性,故可证明元素的非金属性:S>C,D正确;
故合理选项是C。


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是( )

A. 三种酸的电离常数关系:KHA>KHB>KHD
B. 滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C. pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D. 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是可逆反应2A(g)+2B(g)![]() 2C(g)+3D(g)(正反应ΔH>0)的化学反应速率与化学平衡随外界条件改变而变化的关系图。下列条件的改变与图中情况相符的是( )
2C(g)+3D(g)(正反应ΔH>0)的化学反应速率与化学平衡随外界条件改变而变化的关系图。下列条件的改变与图中情况相符的是( )
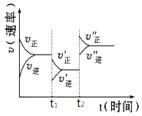
A.t1时,减小了A或B的物质的量浓度
B.t2时,升高了温度
C.t2时,增大了压强
D.t1时,加了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列文字表述与反应方程式对应不正确的是( )
A.将少量铜屑放入浓硝酸中:Cu+4H++2NO![]() =Cu2++2NO2↑+2H2O
=Cu2++2NO2↑+2H2O
B.用醋酸除去水垢:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑
C.将乙烷与溴蒸气混合置于光亮处生成一溴代物:CH3CH3+Br2![]() CH3CH2Br+HBr
CH3CH2Br+HBr
D.氯气和水反应:Cl2+H2O=2H++Cl-+ClO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列我国科技创新的产品设备在工作时,能量转化过程与氧化还原反应有关的是( )
|
|
|
|
①长征三号运载火箭用偏二甲肼为燃料 | ②嫦娥四号月球探测器上的太阳能电池板 | ③和谐号动车以350 km/h飞驰 | ④世界首部可折叠柔屏手机通话 |
A.①②B.③④C.②③D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸。发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云。根据掌握的信息分析,装箱区的危险化学品可能有钾、钠、氯酸钠、硝酸钾、烧碱,硫化碱、硅化钙、三氯乙烯、氯碘酸等。运抵区的危险化学品可能有环己胺、二甲基二硫、甲酸、硝酸铵、氰化钠、4,6-二硝基苯-邻仲丁基苯酚等。
回答下列问题:
(1)在组成NH4NO3、NaCN两种物质的元素中第一电离能最大的是__________(填元素符号),解释原因_____________________________________________
(2)二甲基二硫和甲酸中,在水中溶解度较大的是 (填名称),原因是_______;烧碱所属的晶体类型为______;硫化碱(Na2S)的S2-的基态电子排布式是____________。
(3)硝酸铵中,NO3-的立体构型为 ,中心原子的杂化轨道类型为__________
(4)1mol化合物NaCN中CN-所含的π键数为______,与CN-互为等电子体的分子有 。(CN)2又称为拟卤素,实验室可以用氰化钠、二氧化锰和浓硫酸在加热条件下制得,写成该制备的化学方程式___________。
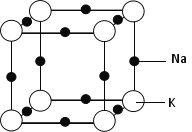
(5)钠钾合金属于金属晶体,其某种合金的晶胞结构如图所示。合金的化学式为____________;晶胞中K 原子的配位数为 ;已知金属原子半径r(Na)=186pm、r(K)=227pm,计算晶体的空间利用率 ________(列出计算式,不需要计算出结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素C的结构简式如图所示:

⑴维生素C分子中—OH原子团的名称是__________________;维生素C__________________溶于水(填“易”或“难”),属于________________ 维生素(填“脂溶性”或“水溶性”)。
⑵维生素C又被称为抗坏血酸,它能促进胶原蛋白形成,所以能防治_____________
⑶一个人每天摄入约100mg维生素C就能满足需要,下列物质中含有丰富维生素C的是____
A.苦瓜 B.鸡蛋 C.豆腐 D.沙丁鱼
⑷“服用维生素C,可使食物中的三价铁离子还原成二价铁离子”这句话说明:维生素C具有_____________性(填“氧化性”或“还原性”);维生素C在这一反应中发生了_____________(填“氧化反应”或“还原反应”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na![]() 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是
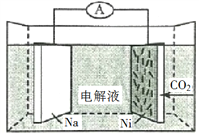
A. 放电时,ClO4-向负极移动
B. 充电时释放CO2,放电时吸收CO2
C. 放电时,正极反应为:3CO2+4e =2CO32-+C
D. 充电时,正极反应为:Na++e=Na
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com