
 将镁、铝的混合物7.5g溶于100mL 4mol/L的H2SO4溶液中,然后再滴加1mol/L的NaOH溶液.请回答:
将镁、铝的混合物7.5g溶于100mL 4mol/L的H2SO4溶液中,然后再滴加1mol/L的NaOH溶液.请回答:分析 根据图象可知,在滴加NaOH溶液到体积V1过程中,没有沉淀生成,说明硫酸有剩余,滴加的NaOH用于中和剩余硫酸,剩余的H2SO4与滴加的NaOH恰好完全反应,溶液是MgSO4、Al2(SO4)3和Na2SO4混合液,根据Mg原子、Al原子、SO42-离子、Na+离子守恒,列方程求算;当滴加NaOH溶液到体积V2时,Al(OH)3完全溶解,沉淀是Mg(OH)2,溶液是Na2SO4和NaAlO2混合液.根据SO42-离子、Na+离子和Al原子守恒,求出n(NaOH),再利用V=$\frac{n}{V}$计算滴入氢氧化钠溶液体积V2;当溶液中Mg2+、Al3+恰好沉淀完全时,即沉淀达到最大值,此时,溶液是Na2SO4溶液,根据SO42-离子和Na+离子守恒有n(Na+)=2n(Na2SO4)=2(H2SO4)求出n(NaOH),再利用V=$\frac{n}{V}$计算需要滴入NaOH溶液的体积.
(1)0~V1段滴入氢氧化钠溶液后没有生成沉淀,说明硫酸过量,加入的氢氧化钠与剩余的硫酸反应生成硫酸钠和水;
(2)剩余的H2SO4与滴加的NaOH恰好完全反应,消耗氢氧化钠溶液V1=100ml,溶液是MgSO4、Al2(SO4)3和Na2SO4混合液,根据Mg原子、Al原子、SO42-离子、Na+离子守恒,列方程求算;
(3)当溶液中Mg2+、Al3+恰好沉淀完全时,即沉淀达到最大值,此时,溶液是Na2SO4溶液,根据SO42-离子和Na+离子守恒有n(Na+)=2n(Na2SO4)=2(H2SO4)求出n(NaOH),再利用V=$\frac{n}{V}$计算需要滴入NaOH溶液的体积,依据金属物质的量金属质量;
(4)依据金属镁和铝物质的量计算电子转移总数;
解答 解:(1)0~V1段,滴入氢氧化钠溶液后没有生成沉淀,说明硫酸过量,滴入的氢氧化钠与硫酸反应生成硫酸钠和水,反应的离子方程式为:H++OH-=H2O,
故答案为:H++OH-=H2O;
(2)当V1=100mL时,此时,溶液是MgSO4、Al2(SO4)3和Na2SO4混合液,
由Na+离子守恒可知,n(Na2SO4)=$\frac{1}{2}$n(Na+)=$\frac{1}{2}$n(NaOH)=$\frac{1}{2}$×0.1L×1mol/L=0.05mol,
设MgSO4为xmol,Al2(SO4)3为ymol,则:
根据Mg原子、Al原子守恒有:24x+27×2y=7.5,
100mL 4mol/L的H2SO4溶液中含有硫酸的物质的量为:4mol/L×0.1L=0.4mol,
根据SO42-离子守恒有:x+3y=0.4-0.05=0.35,
联立方程解得:x=0.2、y=0.05,
所以金属粉末中:n(Mg)=0.2mol,n(Al)=2y=2×0.05mol=0.1mol,
滴加NaOH溶液到体积V2时时,溶液是Na2SO4和NaAlO2混合液,根据SO42-离子、Na+离子和Al原子守恒有:
n(NaOH)=2n(Na2SO4)+n(NaAlO2)=2n(H2SO4)+n(Al)=2×0.4mol+0.1mol=0.9mol,
则V2=$\frac{0.9mol}{1mol/L}$=0.9L=900mL,
故答案为:0.1,900;
(3)当溶液中Mg2+、Al3+恰好沉淀完全时,此时,溶液是Na2SO4溶液,根据SO42-离子和Na+离子守恒有:n(Na+)=2n(Na2SO4)=2(H2SO4)=2×0.4mol=0.8mol,
所以需要氢氧化钠溶液体积为:V(NaOH)=$\frac{0.8ml}{1mol/L}$=0.8L=800mL,
沉淀质量=0.2mol×58g/mol+0.1mol×78g/mol=19.4g
故答案为:800;19.4;
(4)上述计算得到n(Mg)=0.2mol,n(Al)=2y=2×0.05mol=0.1mol,和硫酸全部反应电子转移总数=0.2mol×2+0.1mol×3=0.7mol,
故答案为:0.7.
点评 本题考查了有关混合物反应的计算,题目难度中等,熟练掌握离子性质、明确图象曲线变化的含义为解答此类题的关键,试题侧重考查学生的分析、理解能力及化学计算能力.


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案科目:高中化学 来源: 题型:选择题

| A. | 若要测定所得硫酸铜晶体中结晶水的数目,实验中要用到坩埚、坩埚钳和干燥器等 | |
| B. | 利用Cu(OH)2替代CuO也可调试溶液pH,不影响实验结果 | |
| C. | 洗涤晶体:向滤出晶体的漏斗中加少量冷水浸没晶体,自然流下,重复2-3次 | |
| D. | 用18.4mol/L浓硫酸配制溶解所用4.00mol/L的稀硫酸,玻璃仪器一般只有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40℃时同浓度的H2O2的分解速率一定比10℃时分解速率快 | |
| B. | 实验室用氯酸钾制氧气,增大压强可使反应速率加快 | |
| C. | 改变固体表面积对化学反应速率没有影响 | |
| D. | 在可逆反应中,因受反应限度的影响,研究改变外界条件来提高产率是没有意义的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 双键、三键中一定含有π键 | |
| B. | 成键原子间原子轨道重叠越多,共价键越牢固 | |
| C. | 因每个原子未成对电子数是一定的,故配对原子个数也一定 | |
| D. | 每一个原子轨道在空间都具有方向性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | - |
| 最低价态 | - | - | -2 | - | -4 | -3 | -1 | - | -3 | -1 |
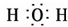 或
或 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2与C2H4 | B. | CO与C2H4 | C. | CO 与C3H6 | D. | H2与C4H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性:HF>HCl>HBr>HI | B. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | ||
| C. | 酸性:H2SO4>H3PO4>HClO4 | D. | 氧化性:O2>S>Se |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com