
| A. | ①② | B. | ①④ | C. | ②④ | D. | ②③④ |
分析 Cu与稀硫酸不反应,因稀硫酸的氧化性较弱,则加具有氧化性的离子或物质可使铜反应而溶解,以此来解答.
解答 解:①因铜不如铁活泼,则铜不能与FeCl2反应,故①错误;
②因Fe2O3能与稀硫酸发生Fe2O3+3H2SO4═Fe2(SO4)3+3H2O,Fe2(SO4)3能与铜粉发生Fe2(SO4)3+Cu═2FeSO4+CuSO4,铜粉溶解,故②正确;
③Zn、Cu、H2SO4形成原电池,加快了反应,但发生的化学反应为Zn+H2SO4═ZnSO4+H2↑,Zn溶解,故③错误;
④因铜与稀HNO3反应,硝酸盐在酸性条件下具有硝酸的强氧化性,发生3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,可知Cu、H+、NO3-能发生氧化还原反应使Cu溶解,故④正确.
故选C.
点评 本题考查物质的性质及氧化还原反应,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将一铝箔放在酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面生成致密的Al2O3薄膜,且Al2O3熔点高于Al |
| B | 向某氯化亚铁溶液中加入Na2O2粉末 | 出现红褐色沉淀 | 加入Na2O2粉末前,原氯化 亚铁溶液已经变质 |
| C | 铜放入稀硫酸中,再加入硝酸钠固体 | 开始无明显现象,后溶液变蓝,有明显的气泡放出,铜溶解 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D |  | 烧杯中有白色胶状沉淀生成 | 非金属性:N>C>Si |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CHClCH2CH3 | B. | CH3CH3 | C. | 甲烷 | D. | CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 扩大铅蓄电池、汞锌锰干电池的生产,满足消费需求 | |
| B. | 采用碳捕集和储存技术,逐步实现二氧化碳的零排放 | |
| C. | 对工业废水、生活污水净化处理,减少污染物的排放 | |
| D. | 催化处理汽车尾气,减轻氮氧化物污染和光化学烟雾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
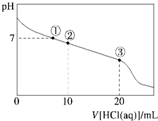 常温下,向20.00mL 0.100mol•L-1 CH3COONa溶液中逐滴加入0.100 0mol•L-1盐酸,溶液的pH与所加盐酸体积的关系如图所示(不考虑挥发).下列说法正确的( )
常温下,向20.00mL 0.100mol•L-1 CH3COONa溶液中逐滴加入0.100 0mol•L-1盐酸,溶液的pH与所加盐酸体积的关系如图所示(不考虑挥发).下列说法正确的( )| A. | 点①所示溶液中:c(CH3COOH)=c(Cl-)>c(OH-)=c(H+) | |
| B. | 点②所示溶液中:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH) | |
| C. | 点③所示溶液中:c(CH3COOH)>c(Na+)>c(H+)>c(CH3COO-) | |
| D. | 整个过程中可能出现:c(H+)+c(Na+)═c(CH3COOH)+c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时CH3OH参与反应的电极为正极 | |
| B. | 充电时电解质溶液的pH逐渐增大 | |
| C. | 放电时负极的电极反应为:2CH3OH-12e-+16OH-═2CO32-+12H2O | |
| D. | 充电时每生成1 mol CH3OH转移6 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从组成看,其成分皆是碱性氧化物 | |
| B. | 沉淀X的成分是SiO2 | |
| C. | 溶液Y中的阳离子主要是Mg2+、Fe3+、H+ | |
| D. | 在溶液Y中加入过量NaOH溶液,先产生沉淀后全部溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代所得产物有6种 | |
| B. | 与 互为同分异构体的芳香族化合物有6种 互为同分异构体的芳香族化合物有6种 | |
| C. | 2-甲基丁烷的一氯取代物共有4种 | |
| D. | 菲的结构简式为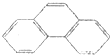 ,它的一硝基取代物有5种 ,它的一硝基取代物有5种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com