
·ÖĪö £Ø1£©¢ŁĶ¼Ļó·ÖĪöĖµĆ÷ŹÆÄ«ÄÜĮæµĶÓŚ½šøÕŹÆ£»ŅĄ¾ŻČ¼ÉÕČČøÅÄīŹĒ1molæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪȶØŃõ»ÆĪļ·Å³öµÄČČĮæ¼ĘĖć£»
¢ŚŅĄ¾ŻŹÆÄ«Č¼ÉÕÉś³ÉŅ»Ńõ»ÆĢ¼ČČ»Æѧ·½³ĢŹ½ŗĶŅ»Ńõ»ÆĢ¼Č¼ÉÕÉś³É¶žŃõ»ÆĢ¼ČČ»Æѧ·½³ĢŹ½½įŗĻøĒĖ¹¶ØĀɼĘĖćµĆµ½ĖłŠčČĆ»Æѧ·½³ĢŹ½£»
£Ø2£©øł¾ŻŌµē³ŲŌĄķ£¬CO2ŌŚÕż¼«·¢Éś»¹Ō·“Ó¦×Ŗ»ÆĪŖ¼×Ķ飬עŅāµē½āÖŹČÜŅŗĪŖ¼īŠŌ£»
£Ø3£©¢ŁŅĄ¾ŻČČ»Æѧ·½³ĢŹ½ŗĶøĒĖ¹¶ØĀɼĘĖćµĆµ½£»
¢ŚĖįŠŌČ¼ĮĻµē³Ų¾Ę¾«¼ģ²āŅĒ£¬·ÖĪö×°ÖĆĶ¼æÉÖŖ¾Ę¾«ŌŚøŗ¼«±»ŃõĘųŃõ»Æ·¢ÉśŃõ»Æ·“Ӧɜ³É“×Ėį£®
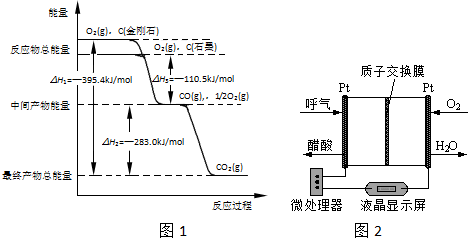
½ā“š ½ā£ŗ£Ø1£©¢ŁĶ¼Ļó·ÖĪöĖµĆ÷ŹÆÄ«ÄÜĮæµĶÓŚ½šøÕŹÆ£¬ĪļÖŹÄÜĮæŌ½µĶŌ½ĪČ¶Ø£¬ĖłŅŌŹÆÄ«ĪČ¶Ø£»ŅĄ¾ŻČ¼ÉÕČČøÅÄīŹĒ1molæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪȶØŃõ»ÆĪļ·Å³öµÄČČĮ棬Ķ¼Ļó·ÖĪö¼ĘĖćµĆµ½Ņ»Ńõ»ÆĢ¼Č¼ÉÕČČ=E2+E3=110.5LKJ/mol+283.0KJ/mol=393.5KJ/mol£»
¹Ź“š°øĪŖ£ŗŹÆÄ«£¬393.5£»
¢ŚŹÆÄ«Č¼ÉÕÉś³ÉŅ»Ńõ»ÆĢ¼ČČ»Æѧ·½³ĢŹ½£ŗa”¢C£Øs”¢ŹÆÄ«£©+$\frac{1}{2}$O2£Øg£©=CO£Øg£©”÷H=-110.5KJ/mol£»
Ņ»Ńõ»ÆĢ¼Č¼ÉÕÉś³É¶žŃõ»ÆĢ¼ČČ»Æѧ·½³ĢŹ½£ŗb”¢CO£Øg£©+$\frac{1}{2}$O2£Øg£©=CO2£Øg£©”÷H=-283.0KJ/mol£»
½įŗĻøĒĖ¹¶ØĀɼĘĖć£¬a-bµĆµ½ĖłŠčČĆ»Æѧ·½³ĢŹ½£ŗC£Øs”¢ŹÆÄ«£©+CO2£Øg£©=2CO£Øg£©”÷H=+172.5kJ•mol-1 £»
¹Ź“š°øĪŖ£ŗC£Øs£©+CO2£Øg£©=2CO£Øg£©”÷H=+172.5 kJ•mol-1£»
£Ø2£©CO2ŌŚÕż¼«·¢Éś»¹Ō·“Ó¦×Ŗ»ÆĪŖ¼×Ķ飬µē¼«·“Ó¦ĪŖ£ŗCO2+8e-+6H2O=CH4+8OH-£¬¹Ź“š°øĪŖ£ŗCO2+8e-+6H2O=CH4+8OH-£»
£Ø3£©¢Ła”¢H2O£Øl£©=H2O£Øg£©”÷H=+44kJ•mol-1
b”¢CO£Øg£©+H2O£Øg£©?CO2£Øg£©+H2£Øg£©”÷H=-41.2kJ•mol-1
c”¢2CO£Øg£©+4H2 £Øg£©?CH3CH2OH£Øg£©+H2O£Øg£©”÷H=-256.1kJ•mol-1
ŅĄ¾ŻøĒĖ¹¶ØĀÉc-b”Į2-3aµĆµ½£ŗ2CO2£Øg£©+6H2£Øg£©?CH3CH2OH£Øg£©+3H2O£Øl£©”÷H=-305.7kJ•mol-1 £»
¹Ź“š°øĪŖ£ŗ-305.7kJ•mol-1 £»
¢Ś¾Ę¾«¼ģ²āŅĒ£¬·ÖĪö×°ÖĆĶ¼æÉÖŖ¾Ę¾«ŌŚøŗ¼«±»ŃõĘųŃõ»Æ·¢ÉśŃõ»Æ·“Ӧɜ³É“×Ėį£¬CH3CH2OH-4e-+H2O=4H++CH3COOH£»
¹Ź“š°øĪŖ£ŗCH3CH2OH-4e-+H2O=4H++CH3COOH£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ·“Ó¦ÄÜĮæ±ä»Æ£¬Ōµē³Ų”¢µē½ā³ŲŌĄķ·ÖĪöÓ¦ÓĆ£¬ČČ»Æѧ·½³ĢŹ½”¢µē½ā·“Ó¦·½³ĢŹ½µÄŹéŠ“Ź½½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®


 Š”ѧÄÜĮ¦²āŹŌ¾ķĻµĮŠ“š°ø
Š”ѧÄÜĮ¦²āŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗÓÄĻŹ”ø߶žÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
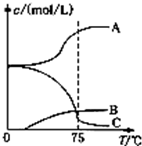
25”ꏱ£¬ŌŚĢå»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ£¬ĘųĢ¬ĪļÖŹA”¢B”¢CµÄĪļÖŹµÄĮæn(mo1)Ėꏱ¼ätµÄ±ä»ÆČēĶ¼2-10-2ĖłŹ¾”£ŅŃÖŖ“ļĘ½ŗāŗ󣬽µµĶĪĀ¶Č£¬AµÄ×Ŗ»ÆĀŹ½« Ōö“ó”£
Ōö“ó”£

(1)øł¾ŻĶ¼ 2-10-2Źż¾Ż£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½________________£»“Ė·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½K=______________”£“Ó·“Ó¦æŖŹ¼µ½“ļµŚŅ»“ĪĘ½ŗāŹ±µÄĘ½¾ł·“Ó¦ĖŁĀŹv(A)ĪŖ_________”£
2-10-2Źż¾Ż£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½________________£»“Ė·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½K=______________”£“Ó·“Ó¦æŖŹ¼µ½“ļµŚŅ»“ĪĘ½ŗāŹ±µÄĘ½¾ł·“Ó¦ĖŁĀŹv(A)ĪŖ_________”£
(2)ŌŚ5”«7minÄŚ£¬ČōKÖµ²»±ä£¬Ōņ“Ė“¦ĒśĻß±ä»ÆµÄŌŅņŹĒ________________”£
(3)Ķ¼2-10-3±ķŹ¾“Ė·“Ó¦µÄ·“Ó¦ĖŁĀŹvŗĶŹ±¼ätµÄ¹ŲĻµ”£ø÷½×¶ĪµÄĘ½ŗā³£ŹżČēĻĀ±ķĖłŹ¾£ŗ
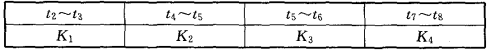
øł¾ŻĶ¼2-10-3ÅŠ¶Ļ£¬ŌŚt3ŗĶt6Ź±æĢøıäµÄĶā½ēĢõ¼ž·Ö±šŹĒ__________ŗĶ____________£»K1”¢K2”¢K3”¢K4Ö®¼äµÄ¹ŲĻµĪŖ__________(ÓĆ”°>”±”°<”±»ņ”°=”±Į¬½Ó)”£Ę½ŗāŹ±AµÄ×Ŗ»ÆĀŹ×ī“óµÄŅ»¶ĪŹ±¼äŹĒ____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆ¼ÓČČ”¢³ĘÖŲµÄ·½·Ø¼ų±šNa2CO3¹ĢĢåŗĶNaHCO3¹ĢĢå | |
| B£® | ÓĆŃęÉ«·“Ó¦¼ų±šNaCl¹ĢĢåŗĶNaOH¹ĢĢå | |
| C£® | ijČÜŅŗÖŠµĪ¼ÓŃĪĖįÄܲśÉśĪŽÉ«ĘųĢ壬øĆĘųĢåÄÜŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£¬ŌņŌČÜŅŗÖŠŅ»¶Øŗ¬CO32- | |
| D£® | ĻņijČÜŅŗÖŠ¼ÓČėBaCl2ČÜŅŗ³öĻÖ°×É«³Įµķ£¬ŌŁ¼ÓČėHClČÜŅŗ£¬°×É«³Įµķ²»Čܽā£¬ŌņøĆČÜŅŗÖŠæĻ¶ØÓŠSO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ĀČĖįÄĘ£ØNaClO3£©ŹĒĪŽ»śŃĪ¹¤ŅµµÄÖŲŅŖ²śĘ·Ö®Ņ»£®
ĀČĖįÄĘ£ØNaClO3£©ŹĒĪŽ»śŃĪ¹¤ŅµµÄÖŲŅŖ²śĘ·Ö®Ņ»£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģ¼ĖįµÄµēĄė·½³ĢŹ½£ŗH2CO3ØT2H++CO32- | |
| B£® | NaHSO4£ØČÜŅŗ£©µÄµēĄė£ŗNaHSO4ØTNa++H++SO42- | |
| C£® | ŃĒĮņĖįÄĘĖ®½āµÄĄė×Ó·½³ĢŹ½£ŗSO32-+2H2O?H2SO3+2OH- | |
| D£® | HCO3-µÄĖ®½ā·½³ĢŹ½ĪŖ£ŗHCO3-+H2O?CO32-+H3O+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«µČĪļÖŹµÄĮæµÄKHC2O4ŗĶH2C2O4ČÜÓŚĖ®Åä³ÉČÜŅŗ£ŗ2c£ØK+£©ØTc£ØHC2O4-£©+c£ØH2C2O4£© | |
| B£® | 0.1 mol•L-1NH4ClČÜŅŗÓė0.1 mol•L-1°±Ė®µČĢå»ż»ģŗĻ£ØpH£¾7£©£ŗc£ØNH3•H2O£©£¾c£ØNH${\;}_{4}^{+}$£©£¾c£ØCl-£©£¾c£ØOH-£© | |
| C£® | 0.1mol/LµÄCH3COOHČÜŅŗ¼ÓĖ®Ļ”ŹĶ£¬$\frac{c£Ø{H}^{+}£©}{c£ØC{H}_{3}CO{O}^{-}£©}$µÄ±ČÖµ½«Ōö“ó | |
| D£® | 0.1mol/LCH3COONaČÜŅŗÓė0.15mol/LHClµČĢå»ż»ģŗĻ£ŗc£ØCl-£©£¾c£ØH+£©£¾c£ØNa+£©£¾c£ØCH3COO-£©£¾c£ØOH-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | $\frac{18}{{N}_{A}}$ | B£® | $\frac{18}{{N}_{A}}$g•mol-1 | C£® | 18NA g | D£® | $\frac{18}{{N}_{A}}$g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 22.4g | B£® | 11.2g | C£® | 20.4g | D£® | 5.6g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹµŃéŹŅ±£“ęµēŹÆŹ±Ó¦×¢ŅāĆÜ·ā£¬²¢ÖĆÓŚŅõĮ¹øÉŌļ“¦ | |
| B£® | ÉĻŹö·“Ó¦²śÉś1molC2H2ĘųĢåŌŚ³£ĪĀ³£Ń¹ĻĀĢå»żĪŖ2.24L | |
| C£® | µēŹÆÓėĖ®·“Ó¦²»ŹĒŃõ»Æ»¹Ō·“Ó¦ | |
| D£® | ²śĪļC2H2ŹōÓŚÓŠ»śĪļ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com