
| A. | 食物发霉 | B. | 冰雪融化 | C. | 铜像生锈 | D. | 聚沙成塔 |
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:选择题
| A. | Na放入水中,产生气体:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 用催化法处理汽车尾气中的CO和NO:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2 | |
| C. | NaOH溶液不能保存在玻璃塞的试剂瓶中:SiO2+2OH-═SiO32-+H2O | |
| D. | 红热的铁丝与水蒸汽接触,表面形成黑色保护层:2Fe+3H2O(气)$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 碳酸钠溶液中加入氯化钙溶液产生沉淀 | |
| B. | 铜粉在空气中加热变成黑色粉末 | |
| C. | 石灰石溶于盐酸并产生无色无味的气体 | |
| D. | 液氢在空气中变为氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ||||||||
| 2 | N | O | F | |||||
| 3 | Na | Si | Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱常用于治疗胃酸过多 | |
| B. | 硫酸亚铁可用作缺铁性贫血的补血剂 | |
| C. | 用明矾进行自来水的杀菌消毒 | |
| D. | 碳酸钙不能用作人体补钙剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 碳酸的酸性比硅酸强 | |
| B. | 136C表示该元素的相对原子质量近似为13,核电荷数为6 | |
| C. | 共价键必然存在于共价化合物中 | |
| D. | X、Y+、Z-三种粒子的电子层结构相同,则其质子数一定不相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液态氧、烧碱、碘酒 | B. | 白磷、生石灰、熟石灰 | ||
| C. | 铁、干冰、氯化氢 | D. | 氮气、空气、胆矾 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
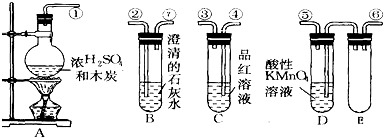
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
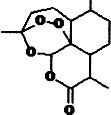 化学在材料科学、生命科学、能源科学等诸多领域发挥着重要的作用.
化学在材料科学、生命科学、能源科学等诸多领域发挥着重要的作用.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com