
【题目】从某含有FeCl2、FeCl3、CuCl2的工业废液中回收铜并制备氯化铁晶体的流程如下:则下列说法正确的是
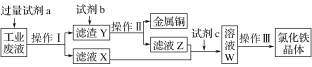
A. 试剂a是铁、试剂b是稀硫酸
B. 操作Ⅰ、操作Ⅱ、操作Ⅲ所用仪器相同
C. 试剂c是氯气,相应的反应为: 2Fe2++Cl2===2Cl-+2Fe3+
D. 用酸性KMnO4溶液可检验溶液W中是否还有Fe2+
【答案】C
【解析】
含有FeCl2、FeCl3、CuCl2的工业废液中加入过量的铁粉,得到氯化亚铁溶液和铁粉、铜粉的混合物,铁粉、铜粉的混合物中加入过量盐酸可得到金属铜和氯化亚铁溶液,氯化亚铁溶液中通入过量氯气得到氯化铁溶液,氯化铁溶液在氯化氢气流中蒸发得氯化铁晶体。
根据以上分析,试剂a是铁、试剂b是稀盐酸,故A错误;操作Ⅰ是过滤、操作Ⅱ是过滤、操作Ⅲ是蒸发,所用仪器不相同,故B错误;试剂c是氯气,氯气与氯化亚铁反应的离子方程式是: 2Fe2++Cl2===2Cl-+2Fe3+,故C正确;酸性KMnO4溶液可以氧化Fe2+、Cl-,所以不能用酸性KMnO4溶液检验溶液W中是否还有Fe2+,故D错误。


科目:高中化学 来源: 题型:
【题目】下列关于离子化合物和共价化合物的说法正确的是( )
A.共价化合物中可能含离子键
B.离子化合物中可能不含金属元素
C.共价化合物溶于水不能导电
D.第ⅠA族元素与第ⅦA族元素形成的化合物一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验所述的变化过程与氧化还原反应无关的是
A | B | C | D | |
实验 | NaOH 溶液滴入FeSO4 溶液中 | 石蕊溶液滴入氯水中 | 向 K2Cr2O7 溶液 中滴加浓硫酸 | CO2 通入 Na2O2 |
现象 | 产生白色沉淀,最 终变为红褐色 | 溶液变红,随后迅速褪色 | 溶液黄色变浅, 橙色加深 | 固体逐渐变白 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是一种性能优异的高分子材料,其结构简式为:
![]()
已被广泛应用于声、热、光的传感等方面。它是由CH≡CH、(CN)2、CH3COOCHCH=CH2三种单体通过适当反应形成的。由H的结构简式分析合成过程中发生反应的类型是:①加成反应;②取代反应;③缩聚反应; ④加聚反应 ( )
A. ①② B. ①③ C. ①④ D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由铜、锌和稀盐酸组成的原电池中,铜是________极,发生________反应,电极反应式是________;锌是________极,发生________反应,电极反应式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室进行二氧化硫制备与性质实验的组合装置如图所示,部分夹持装置未画出。

请回答下列问题:
(1)在组装好装置后,首先要进行的实验操作为_________________________________。
(2)为检验SO2与Na2O2的反应是否有氧气生成,装置B中盛放的试剂X应为________,装置D中碱石灰的作用是_______________________________________________。
(3)关闭弹簧夹2,打开弹簧夹1,注入70%的硫酸至浸没三颈烧瓶中的固体,检验SO2与Na2O2反应是否有氧气生成的操作及现象是_____________________________________。
(4)关闭弹簧夹1,打开弹簧夹2,残余气体进入装置E、F、G中,能说明I-的还原性弱于SO2的现象为_________________。发生反应的离子方程式是______________________。
(5)为了验证装置E中SO2与FeCl3发生了氧化还原反应,某学生设计了如下实验:取少量装置E中的溶液于试管中,向其中加入稀硝酸酸化的BaCl2溶液,产生白色沉淀,并由此判断SO2与FeCl3发生了氧化还原反应。上述方案是否合理?________(填“合理”或“不合理”),原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色溶液中大量共存的一组离子是( )
A.Cu2+、SO42-、OH-、K+B.Fe3+、NO3-、Cl-、H+
C.K+、CO32-、Cl-、H+D.H+、Na+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有OH-、CO32-、[Al(OH)4]-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸时,发现生成沉淀的物质的量随盐酸溶液的体积变化如图所示。下列说法正确的是
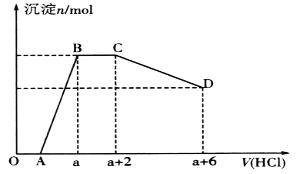
A. BC段是OH-与盐酸反应
B. 反应后最终溶液中的溶质只有NaC1
C. 原溶液中含有CO32-与[Al(OH)4]-的物质的量之比为3:4
D. 原溶液中一定含有的离子是Na+、OH-、SiO32-、SO42-、[A1(OH)4]-、CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com