
����Ŀ����ҵ���Ƚ�úת��ΪCO��������CO��ˮ������Ӧ��H2ʱ����������ƽ�⣺CO(g)��H2O(g)CO2(g)��H2(g)��
(1)ƽ�ⳣ���ı���ʽK=_________________________
(2)��1L�����ܱ������г���CO��H2O(g)��ij�¶�ʱ��ò����������±���
t/min | 0 | 1 | 2 | 3 | 4 |
n(H2O)/mol | 1.20 | 1.04 | 0.90 | 0.70 | 0.70 |
n(CO)/mol | 0.80 | 0.64 | 0.50 | 0.30 | 0.30 |
��ӷ�Ӧ��ʼ��2minʱ����H2��ʾ�ķ�Ӧ����Ϊ__________�����¶��·�Ӧ��ƽ�ⳣ��K��________(С�������2λ��Ч����)��
(3)��֪�÷�Ӧ�ڲ�ͬ���¶��µ�ƽ�ⳣ����ֵ�ֱ�Ϊ
t/�� | 700 | 800 | 830 | 1000 | 1200 |
K | 1.67 | 1.19 | 1.00 | 0.60 | 0.38 |
�ٸ��ݱ��е������жϣ��÷�ӦΪ________(��������������������)��Ӧ��
��800������2L�����ܱ������г���1molCO(g)��1molH2O(g)��2molCO2(g)��2molH2(g)����ʱv��_______v�� (����>����<����������)��
���𰸡�![]() 0.15 mol��L��1��min��1 1.19 ���� ��
0.15 mol��L��1��min��1 1.19 ���� ��
��������
(1)ƽ�ⳣ���ı���ʽK=![]() ��
��
(2)���ݱ�����2min��CO�ķ�Ӧ���ʣ����ݷ�Ӧ����֮�ȵ��ڷ�Ӧ����ϵ��֮�ȣ���v(H2)=v(CO)����Ӧ���е�3minʱ����Ӧ�ﵽƽ��״̬��������ʽ������
(3)�������¶ȣ�ƽ�ⳣ����С��ƽ�������ƶ����ݴ˷����жϡ�
�ڸ�������������ʽ����Qc����ͬ�¶��µ�ƽ�ⳣ��K�Ƚϣ��жϷ�Ӧ���еķ�����ȷ�����淴Ӧ���ʵĴ�С��
(1)��֪��Ӧ��CO(g)��H2O(g)CO2(g)��H2(g)��ƽ�ⳣ���ı���ʽK=![]() =
=![]() ��
��
(2)���ݱ�����ӷ�Ӧ��ʼ��2minʱ��CO�����ʵ����ı仯��Ϊ0.3mol�����Ϊ1L����CO�����ʵ���Ũ�ȵı仯��Ϊ0.3mol/L��2min �ڣ�v(CO)=![]() =0.15 mol��L��1��min��1.����Ӧ����֮�ȵ��ڷ�Ӧ����ϵ��֮�ȣ���v(H2)=v(CO)=0.15 mol��L��1��min��1��
=0.15 mol��L��1��min��1.����Ӧ����֮�ȵ��ڷ�Ӧ����ϵ��֮�ȣ���v(H2)=v(CO)=0.15 mol��L��1��min��1��
��Ӧ���е�3minʱ����Ӧ�ﵽƽ��״̬��������ʽ��

��ƽ�ⳣ��K=![]() ��1.19��
��1.19��
(3)���ɱ������ݿ�֪�������¶ȣ�ƽ�ⳣ����С��ƽ�������ƶ���������ӦΪ���ȷ�Ӧ��
��800�棬��2L�����ܱ������г���1molCO(g)��1molH2O(g)��2molCO2(g)��2molH2(g)����Qc=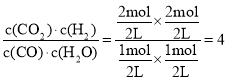 ��800��ʱ��K=1.19����Qc��K��ƽ���������ƶ�����v����v����
��800��ʱ��K=1.19����Qc��K��ƽ���������ƶ�����v����v����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1) д��CO2�Ŀռ乹�ͣ�___________��
(2) д��Na3N�ĵ���ʽ��____________________��
(3) д��C2H6O�Ļ�ѧ���ƣ�______________________��
(4) д����ϩ��ʵ��ʽ��_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳɰ�������Ӧԭ��Ϊ��N2 (g)+3H2(g)2NH3(g) ��H=-92.4 kJ��mol-1
(1)T �� ʱ����Ӧ�ﵽƽ�⣬��� ��(NH3)��0.12 mol��L-1��min -1
�� ��(N2)��____mol��L-1��min -1
�� ��ѧƽ�ⳣ������ʽ K��_____
(2)������������ͬʱ��ͼΪ�ֱ�ⶨ��ͬѹǿ����ͬ�¶��£�N2 ��ƽ��ת���ʡ�
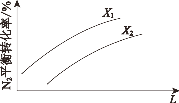
L ��ʾ______������ X1______ X2(����>������<)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2018��5�������о���Ա�ɹ�ʵ���ڳ��³�ѹ���õ�����ˮ��������ԭ������ͼ��ʾ��
����˵����ȷ���ǣ� ��
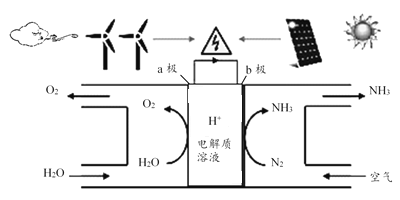
A. ͼ������ת����ʽֻ��2��
B. H+��a�����ƶ�
C. b�������ĵ缫��ӦΪ��N2+6H++6e��=2NH3
D. a����ÿ����22.4LO2�����缫�ĵ�����һ��Ϊ4��6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ������һ�����ʵ���Ũ����Һ�Ĺ���ʾ��ͼ������˵���д������( )

A.�����Ƶ�Na2CO3��Һ�����ʵ���Ũ��Ϊ1.0 mol �� L��1
B.����2�ǽ��ܽⲢ���������µ�Na2CO3��Һת�Ƶ�����ƿ��
C.����4������ӣ���ʹ�����Һ��Ũ��ƫ��
D.����5�У�����ҡ�Ⱥ���Һ����ڿ̶��ߣ�������ˮ��Һ����̶�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��������������������أ������ѧ����ѧ֪ʶ�����������
(1)����������ұ����Ӧ����ʱ���õ�ⷨ����___________��
a��Cu2S b��NaCl c��Fe2O3 d��HgS
(2) �����鶾�����ҹ�����ǧ����ʷ��������Ҫ���ڼ����Ƿ��к���Ԫ�ص��ж����ʡ��䷴Ӧԭ��֮һΪ��4Ag��2H2S��O2=2Ag2S��2H2O���������ɫ��������ʢ��ʳ��ˮ������������һ��ʱ����ɸ�ԭ��ԭ�����γ���ԭ��أ���ԭ��صĸ�����Ӧ��Ϊ��______��
(3)ijͬѧ���һ��ȼ�ϵ��(����ͼ��ʾ)��Ŀ����̽���ȼҵԭ���ʹ�ͭ�ľ���ԭ����������װ����XΪ�����ӽ���Ĥ��

��ͨ�����ĵ缫Ϊ________(��������������������)���õ缫��ӦʽΪ___________��
����װ�ù���һ��ʱ���ϻ�ѧ����������缫���������̪����ԭ��____________��
�������ͭ�к���п���������ʣ���װ���з�Ӧһ��ʱ�䣬����ͭ��ҺŨ�Ƚ�________(��������������С������������)����ͭ�缫�ϵĵ缫��ӦʽΪ_________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ե�ʯ��[��Ҫ�ɷ�ΪCa(OH)2��CaCO3]Ϊԭ���Ʊ�KClO3���������£�
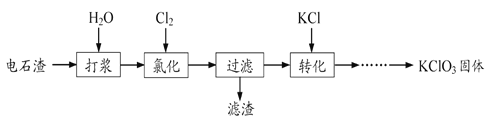
����˵����ȷ����
A.���裬����ʯ�����Ƴ���Һ
B.�Ȼ����裬��������Ҫ��Ӧ2Ca(OH)2 + 2Cl2 = Ca(ClO)2 + CaCl2 +2H2O
C.�Ȼ����̼ӿ�������ͨ�����ʣ����������KClO3�IJ���
D.KClO3�����п��ܻ��� KCl��KClO������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ��ˮ���������Ҫ����֮һ�ǿ������������䲿������ͼ���£�
![]()
�����ƶϲ���������(����)
A. �ȿ����ܴ��������������ӷ�������
B. SO2������ķ�Ӧ����ʽ��SO2��2H2O��Br2=H2SO4��2HBr
C. ������ѭ�����õ�������SO2��Br2��Cl2��
D. û�в���ֱ������Br2�ĺ�ˮ�õ���������Ҫ��Ϊ�˽���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20ml0.1mol/L��ˮ��Һ�еμ����ᣬ��Һ��ˮ�����������Ũ���������������仯��ͼ��ʾ��������˵����ȷ���ǣ� ��
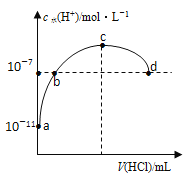
A.b��d����Ϊǡ����ȫ��Ӧ��
B.c����Һ��c(NH4+)=c(Cl-)
C.a��b֮�������һ�㣺c(Cl-)>c(NH4+)��c(H+)>c(OH-)
D.�����£�0.1mol/L��ˮ�ĵ��볣��KԼΪ1��10-5mol/L
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com