
以化学平衡移动原理为依据,解释以下事实。
(1)在氨水中加入氢氧化钠溶液,有氨气逸出
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)合成氨工业中将氨气液化,可以提高氨的产量
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)用热水溶解碳酸钠晶体(Na2CO3·10H2O),可提高去污能力
________________________________________________________________________
________________________________________________________________________。
(4)打开冰冻啤酒倒入玻璃杯,杯中立即泛起大量泡沫
________________________________________________________________________
________________________________________________________________________。
解析:根据化学平衡移动原理,讨论外界条件对化学平衡的影响,确定平衡移动的方向,这是解题的依据。
答案:(1)氨水中存在两个平衡,溶解平衡和电离平衡:
NH3+H2O NH3·H2O
NH3·H2O NH
NH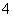 +OH-,当加入NaOH溶液,平衡体系中OH-的浓度增大,使上述平衡向逆反应方向移动,故氨气逸出
+OH-,当加入NaOH溶液,平衡体系中OH-的浓度增大,使上述平衡向逆反应方向移动,故氨气逸出
(2)合成氨的反应:N2(g)+3H2(g) 2NH3(g)。氨气在混合气体中有一定含量,若将氨气液化,使氨气不断离开平衡体系,致使合成氨的反应向正反应方向移动,故可提高氨的产量
2NH3(g)。氨气在混合气体中有一定含量,若将氨气液化,使氨气不断离开平衡体系,致使合成氨的反应向正反应方向移动,故可提高氨的产量
(3)碳酸钠晶体溶于水去油污,原因是碳酸钠水解呈碱性:CO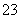 +H2O
+H2O HCO
HCO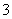 +OH-,HCO
+OH-,HCO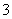 +H2O
+H2O H2CO3+OH-。盐的水解反应是中和反应的逆反应,是吸热反应,升高温度使水解平衡向正反应方向移动,水解程度增大,碱性增强,从而提高去污能力
H2CO3+OH-。盐的水解反应是中和反应的逆反应,是吸热反应,升高温度使水解平衡向正反应方向移动,水解程度增大,碱性增强,从而提高去污能力
(4)饮料在日常生活中相当普遍,其中含有一定量的化学物质,啤酒中CO2就是其中的一种。CO2在水中存在溶解平衡:CO2(g)  CO2(aq),化学平衡:CO2+H2O
CO2(aq),化学平衡:CO2+H2O H2CO3,上述平衡受压力和温度影响,打开冰冻啤酒后,温度升高压强减小,均使两平衡向逆反应方向移动,CO2(g)的量增大,所以,杯中立即泛起大量泡沫
H2CO3,上述平衡受压力和温度影响,打开冰冻啤酒后,温度升高压强减小,均使两平衡向逆反应方向移动,CO2(g)的量增大,所以,杯中立即泛起大量泡沫


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
|
制太阳能电池需要高纯硅,工业上用粗硅制高纯硅可通过以下反应实现
①Si+3HCl(气)=====SiHCl3(气)+H2 ②SiHCl3(气)+H2=====Si+3HCl(气)
对上述两个反应的叙述错误的是( )。
A.都是置换反应 B.都是氧化还原反应
C.反应中硅元素都被还原 D.都不是离子反应
查看答案和解析>>
科目:高中化学 来源: 题型:
关于催化剂的叙述,正确的是( )
A.催化剂在化学反应前后性质不变
B.催化剂在反应前后质量不变,故催化剂不参加化学反应
C.使用催化剂可以改变反应达到平衡的时间
D.催化剂可以提高反应物的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、黏合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:CH3COOH+C2H5OH CH3COOC2H5+H2O。请根据要求回答下列问题:
CH3COOC2H5+H2O。请根据要求回答下列问题:
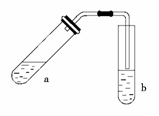
(1)试管a中需加入浓硫酸、冰醋酸和乙醇各2 mL,正确的加入顺序及操作是
________________________________________________________________________。
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是
________________________________________________________________________。
(3)实验中加热试管a的目的是:①__________________;
②________________________________________________________________________。
(4)此反应以浓硫酸为催化剂,可能会造成____________、____________________等问题。
(5)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)。
| 同一反应时间 | 同一反应温度 | ||||
| 反应温度/℃ | 转化率/% | 选择性/% | 反应时间/h | 转化率/% | 选择性/% |
| 40 | 77.8 | 100 | 2 | 80.2 | 100 |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
| 选择性100%表示反应生成的产物是乙酸乙酯和水 |
①根据表中数据,下列________(填字母)为该反应的最佳条件。
A.120 ℃,4 h B.80 ℃,2 h
C.60 ℃,4 h D.40 ℃,3 h
②当反应温度达到120 ℃时,反应选择性降低的原因可能为
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在一固定容积的密闭容器中发生反应:2NO2(g) 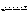 N2O4(g),达平衡时,再向容器内通入一定量的NO2,重新达到平衡后,与第一次平衡相比,NO2的体积分数( )
N2O4(g),达平衡时,再向容器内通入一定量的NO2,重新达到平衡后,与第一次平衡相比,NO2的体积分数( )
A.不变 B.增大
C.减小 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学—选修有机化学基础】(15分)
现有分子式为CnH8O2X2的物质M,可发生如下所示转化:
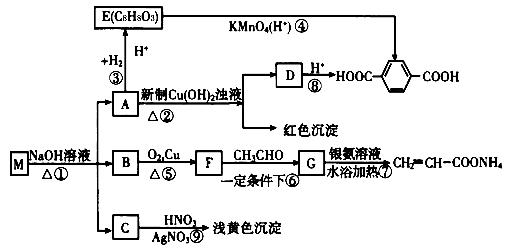
已知:①物质B在质谱分析中,在质谱图显示存在多种质荷比不相同的粒子,其中质荷比最大的为32,物质B在核磁共振氢谱分析中,有两个吸收峰,吸收峰面积之比为3∶1。
②两个—OH同时连在一个C原子上,结构不稳定,会自动失水,如:
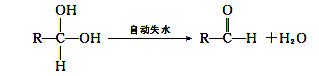
请回答下列问题:
(1)n值为 ,X为 (填元素符号)。
(2)③的反应类型: 。
(3)写出E、G的结构简式;
E: ; G: 。
(4)写出下列反应的化学方程式:
A→D: ;
B→F: 。
(5)写出一种符合下列条件的E的同分异构体的结构简式
①属于酯
②属于酚
③不能发生银镜反应
④苯环上的一溴代物只有两种 。
查看答案和解析>>
科目:高中化学 来源: 题型:
2001年诺贝尔化学奖授予“手性碳原子的催化氢化、氧化反应”研究领域作出贡献的美、日三位科学家。在有机物分子中,当碳原子连有4个不同的原子或原子团时,这种碳原子称为“手性碳原子”,凡具有一个手性碳原子的化合物一定具有光学活性。下列分子中含有“手性碳原子”的是
A.CBr2F2 B.CH3CH2OH C.CH3CH2CH3 D.CH3CH(OH)COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
.将SO2分别通入下列4种溶液中,有关说法正确的是
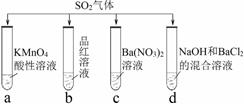
A.试管a中实验可以证明SO2具有漂白性 B.试管b中溶液褪色,说明SO2具有强氧化性
C.试管c中能产生白色沉淀,说明SO2具有还原性
D.试管d中能产生白色沉淀,该沉淀完全溶于稀硝酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com