
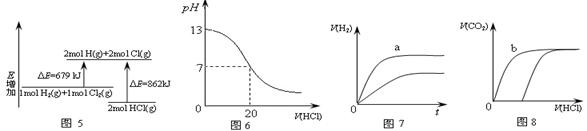
| A��ͼ5��ʾ��ѧ��ӦH2(g)+Cl2(g)=2HCl(g)�������仯����÷�Ӧ�ķ�Ӧ�ȡ�H =183kJ��mol-1 |
| B��ͼ6��ʾ����ʱ��0.1mol��L-1����ζ�20mL0.1mol��L-1NaOH��Һ����ҺpH�����������仯 |
| C��ͼ7��ʾ�����pH����ͬ��HCl��CH3COOH������Һ�У��ֱ����������п������H2�������ʱ��ı仯����a��ʾCH3COOH��Һ |
| D��ͼ8��ʾ10mL0.1mol/LNa2CO3��NaHCO3������Һ�У��ֱ�μ�0.1mol/LHCl������CO2���������������ı仯����b��ʾNa2CO3��Һ |


 ��ɢ˼ά�¿���ϵ�д�
��ɢ˼ά�¿���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��ˮ�ⷴӦ�ǵ��͵Ŀ��淴Ӧ��ˮ�ⷴӦ�Ļ�ѧƽ�ⳣ����Ϊˮ�ⳣ��(��Kh��ʾ)��Na2CO3��һ��ˮ�ⷴӦ��ˮ�ⳣ���ı�ʾʽ Kh�� |
B��HS����������ӷ���ʽ��HS����H2O H3O����S2�� H3O����S2�� |
C��N2(g)��3H2(g) 2NH3(g) ��H��0��������������ʱ�����¶ȣ���Ӧ���ʣ�(H2)����������ƽ��ת���ʱ�С 2NH3(g) ��H��0��������������ʱ�����¶ȣ���Ӧ���ʣ�(H2)����������ƽ��ת���ʱ�С |
| D��CO(g)��ȼ������283.0 kJ��mol��1�����ʾCO(g)��ȼ���ȵ��Ȼ�ѧ����ʽΪ�� |
 O2(g)��CO2(g)����H����283.0 kJ��mol��1
O2(g)��CO2(g)����H����283.0 kJ��mol��1�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
 CO2(g)��H2(g)���õ������������ݣ�
CO2(g)��H2(g)���õ������������ݣ�| ʵ���� | �¶ȡ� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ȫ�� | B���ۢܢݢ� | C���ڢܢݢ� | D���٢ڢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
 CH3OH(g) ��H1����116 kJ��mol-1
CH3OH(g) ��H1����116 kJ��mol-1| A����ʱ��CH3OH�뷴Ӧ�������� |
| B�����ͷ�Ӧ�¶� |
| C��������ϵѹǿ |
| D��ʹ�ø�Ч���� |


 CH3OH(g) ��ƽ�ⳣ��K = ��
CH3OH(g) ��ƽ�ⳣ��K = ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
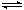 CH3OH(g)+H2O(g)��ijЩ��ѧ���ļ����������±���
CH3OH(g)+H2O(g)��ijЩ��ѧ���ļ����������±���| ��ѧ�� | C��C | C��H | H��H | C��O | C=O | H��O |
| ����/kJ��mol-1 | 348 | 413 | 436 | 358 | 750 | 463 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
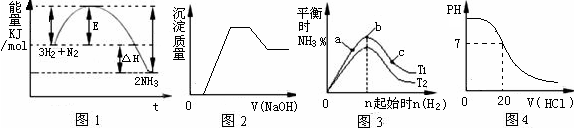
| A����ͼ1��֪�ϳɰ���ӦΪ�Է���Ӧ�������ʵ��Ĵ�����E�͡�H����С |
| B��ͼ2��ʾ����H+��Mg2+��Al3+��NH4+�м���NaOH��Һ��������������ı仯��ϵ |
| C��ͼ3��ʾ�ϳɰ���Ӧ�������������������£��ı���ʼ��n��H2���Դ˷�Ӧƽ���Ӱ�졣��֪��Ӧ��N2��ת������ߵ���b�㣻T1��T2��K2�� K1��T1��T2��ʾ�¶ȣ�K1��K2��ʾ��Ӧ�¶���ƽ�ⳣ���� |
| D��ͼ4��ʾ25��ʱ����0.1 mol��L-1����ζ�20 mL 0.1 mol��L-1��ˮ��pH�������������ı仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ˮ������ɫ���ľ��壬����������̫���ܵ�� |
| B������0.1 mol/LNaCl��Һ��������ʱ���ӣ���������ҺŨ��ƫС��������������ȷ�� |
| C����ˮ�м���������������ƶ���ʹˮ�ĵ���ƽ�������ƶ���ˮ�����ӻ����� |
| D����֪��(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) ��H="+74.9" kJ��mol-1����˸÷�Ӧһ�������Է����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
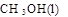 +
+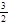
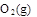 =
= 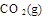 + 2
+ 2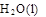 ��H = ��725.5 kJ��mol��1
��H = ��725.5 kJ��mol��1
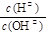 = 1��10�� 6 �������Һ��pHΪ____����Һ�е����ʵ������������Ũ��ԼΪ ���� pH = 4��������ҺV1 L�� 0.01 mol��L��1��ˮV2 L��ϣ��������ҺpH = 7����V1��V2�Ĺ�ϵΪ��V1 V2���>������<����=������
= 1��10�� 6 �������Һ��pHΪ____����Һ�е����ʵ������������Ũ��ԼΪ ���� pH = 4��������ҺV1 L�� 0.01 mol��L��1��ˮV2 L��ϣ��������ҺpH = 7����V1��V2�Ĺ�ϵΪ��V1 V2���>������<����=�������鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com